
����Ŀ��NH4Al��SO4��2��ʳƷ�ӹ�����Ϊ��ݵ�ʳƷ���Ӽ������ڱ���ʳƷ��NH4HSO4�ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺����ش��������⣺
��1����ͬ�����£�0.1molL��1��NH4Al��SO4��2��c��NH4+��������ڡ��������ڡ���С�ڡ���0.1molL��1NH4HSO4��c��NH4+����
��2����Ϊ0.1molL��1�ļ��ֵ������Һ��pH���¶ȱ仯��������ͼ1��ʾ�� 
�����з���0.1molL��1NH4Al��SO4��2��pH���¶ȱ仯�������� �� ����pH���¶ȱ仯��ԭ������
��20��ʱ��0.1molL��1��NH4Al��SO4��2��2c��SO42������c��NH4+����3c��Al3+��=��ȡ����ֵ��
��3������ʱ����100mL0.1molL��1NH4HSO4��Һ�еμ�0.1molL��1NaOH��Һ����ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ2��ʾ�� �Է���ͼ��a��b��c��d�ĸ��㣬ˮ�ĵ���̶��������㣻��b�㣬��Һ�и�����Ũ���ɴ�С������˳���� ��
���𰸡�
��1����
��2���� NH4Al��SO4��2ˮ��ʹ��Һ������,�����¶�,��ˮ��̶�����,pH��С��10��3mol?L��1
��3��a�� c��Na+����c��SO42������c��NH4+����c��OH����=c��H+��
���������⣺��1��NH4Al��SO4��2��NH4HSO4�е�NH4+������ˮ�⣬����NH4Al��SO4��2��Al3+ˮ�����������NH4+ˮ�⣬HSO4�������H+ͬ������NH4+ˮ�⣬��ΪHSO4���������ɵ�H+Ũ�ȱ�Al3+ˮ�����ɵ�H+Ũ�ȴ�����NH4HSO4��NH4+ˮ��̶ȱ�NH4Al��SO4��2�е�С���ʴ�Ϊ��С�ڣ���2����NH4Al��SO4��2ˮ�⣬��Һ�����ԣ������¶���ˮ��̶�����pH��С�����ϵ�����Ϊ��
�ʴ�Ϊ����NH4Al��SO4��2ˮ��ʹ��Һ�����ԣ������¶ȣ���ˮ��̶�����pH��С��
�ڸ��ݵ���غ㣬�������2c��SO42������c��NH4+����3c��Al3+��=c��H+����c��OH����=10��3 molL��1[c��OH����̫С���ɺ���]���ʴ�Ϊ��10��3 molL��1����3��a��b��c��d�ĸ��㣬���ݷ�Ӧ���Ĺ�ϵ��a��ǡ��������H+����Һ��ֻ�У�NH4��2SO4��Na2SO4��b��c��d������Һ������NH3H2O����NH4��2SO4���Դٽ�ˮ�ĵ��룬��NH3H2O����ˮ�ĵ��룮b����Һ�����ԣ�����Һ���У�NH4��2SO4��Na2SO4��NH3H2O���ֳɷ֣�a��ʱc��Na+��=c��SO42������b��ʱc��Na+����c��SO42����������NԪ����SԪ�صĹ�ϵ�����Եó�c��SO42������c��NH4+������c��Na+����c��SO42������c��NH4+����c��OH����=c��H+����
�ʴ�Ϊ��a��c��Na+����c��SO42������c��NH4+����c��OH����=c��H+����
��1��NH4Al��SO4��2��Al3+ˮ�����������NH4+ˮ�⣬HSO4�������H+ͬ������NH4+ˮ�⣻��2����NH4Al��SO4��2ˮ�⣬��Һ�����ԣ������¶���ˮ��̶�����
�ڸ��ݵ���غ㶨�ɽ��⣻��3��a��b��c��d�ĸ��㣬���ݷ�Ӧ���Ĺ�ϵ��a��ǡ��������H+����Һ��ֻ�У�NH4��2SO4��Na2SO4��b��c��d������Һ������NH3H2O����NH4��2SO4���Դٽ�ˮ�ĵ��룬��NH3H2O����ˮ�ĵ��룮b����Һ�����ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں����ܱ�������ͨ��X��������Ӧ��2X��g��Y��g�����¶�T1��T2��X�����ʵ���Ũ��c��X����ʱ��t�仯��������ͼ��ʾ������������ȷ���ǣ������� 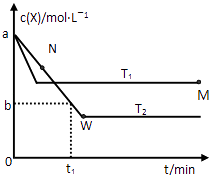
A.�÷�Ӧ���е�M��ų����������ڽ��е�W��ų�������
B.T2�£���0��t1ʱ���ڣ�v��Y��= ![]() molL��1min��1
molL��1min��1
C.M�������Ӧ����V������N����淴Ӧ����V��
D.M��ʱ�ټ���һ����X��ƽ���X��ת���ʼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ľ�ҵ���Ч�ɷ���K2CO3��������������Na����Cl����SO42���ʹ���������ˮ�Ĺ��塣Ϊ�ⶨ����K2CO3�ĺ������������ʵ�飺

���������գ�
��1��ϴ��������Ŀ����_____________________________________��
��2������100 mL��ľ�ҽ���Һ����Ҫʹ�õIJ����������ձ�������������ͷ�ιܡ�______��
��3��ȡ��10.00 mL����Һ���еζ����յ�ʱ��Һ��______ɫ���______ɫ��������ƽ��ʵ���������������ƽ��ֵΪ25.00 mL�������Ʒ��̼��ص���������Ϊ______����ȷ��С�����3λ����
��4����û���ñ�Һ��ϴ�ζ��ܣ���ʵ������___������ƫ��������ƫС��������Ӱ��������
��5��������ͼװ�ã�ͨ����Ӧǰ���������ĸı䣬ȷ��CO2�����������Ҳ���Բⶨ��Ʒ��̼��صĺ�����ʵ��ʱ������Ӧ�����ӷ���ʽΪ_______________________���жϷ�Ӧ��ȫ��������_____________________����Ը�ʵ�鷽������ȱ��������ۡ�________________

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2H��3H���������ⵯ��ԭ�ϡ����й���2H��3H��˵����ȷ����
A.2H��3H����������ͬB.2H��3H��Ϊͬλ��
C.2H��3H��ͬһ�ֺ���D.3Hԭ�ӵĵ�����Ϊ3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Ƚ��У���ȷ��
A.ԭ�Ӱ뾶��Al��Mg��NaB.�ȶ��ԣ�HF��H2O��NH3
C.���ԣ�H2CO3��H2SO4��HClO4D.���ԣ�Al(OH)3��Mg(OH)2��NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ�һ���¶��£����ݻ��̶����ܱ������н��еĿ��淴Ӧ��2NO2![]() 2NO��O2���ﵽƽ��ı�־��
2NO��O2���ﵽƽ��ı�־��
����ͬʱ���ڣ���������������Ϊn mol��L��1��s��1��NO2����������Ϊ2n mol��L��1��s��1
����λʱ��������n mol O2��ͬʱ����2n mol��NO
������������ɫ���ٱ仯�� �����������ܶȱ��ֲ��䡡
����������ƽ����Է����������ٸı䡡��ѹǿ����ʱ��仯���仯
A. �٢ۢݢ� B. �ڢۢ�
C. �٢ۢ� D. �٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����ʽ����ȷ���ǣ�������
A.CH3CO18OC2H5+H2O ![]() CH3COOH��C2H518OH
CH3COOH��C2H518OH
B.����������������Һ���ȣ�CH3CH2Br+NaOH ![]() CH3CH2OH+NaBr
CH3CH2OH+NaBr
C.����ˮ�⣺ ![]() +H2O
+H2O ![]()
![]()
D.��������ͨ�������̼�� ![]() +CO2+H2O��
+CO2+H2O�� ![]() +NaHCO3
+NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ�ѧ��Ӧ�Է��Ե�˵����ȷ����(����)
A. ���ȷ�Ӧһ�����Է����еķ�Ӧ
B. ��Ӧ���Է���Ҫ�ۺϿ����ʱ���ر���������
C. ��ѧ��Ӧ���ر��뷴Ӧ�ķ�����
D. ֻ�в���Ҫ�κ��������ܹ��Զ����еĹ��̲����Է�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2����ɫ���š�����ת��������ɳ�����չ����Ҫս��֮һ��
��1��CO2��Դ֮һ������β��
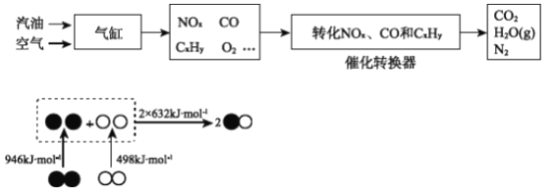

�ٸ�����ͼ��д�������ڲ���NO���Ȼ�ѧ����ʽ________��
��д��ת�������ڴ���������NOx��CO��Ӧ�Ļ�ѧ����ʽ________��
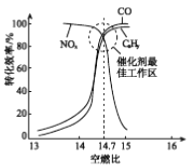
���ڴ�ת�����л�����β��ת��Ч�����ȼ�ȣ�������ȼ����������ȣ��Ĺ�ϵ����ͼ������ȼ��С��14.7���������㣬CxHy��CO���ܱ���ȫ������������ת��Ч�ʽ��ͣ�����ȼ�ȴ���14.7����NOx��ת��Ч�ʽ��ͣ�ԭ����________��
��2������NaOH��Һ���������� CO2
��֪��0.448L CO2���������״������NaOH��Һ������գ��õ�100mL����Na2CO3��NaHCO3������Һ��
��������Һ�м�������BaCl2��Һ�õ������������ˡ�ϴ�ӡ��������Ϊ1.97g��������Һ��c(Na2CO3) = ________������������NaHCO3��BaCl2����Ӧ��
�ڶԸ�����Һ�������ж���ȷ����________��
a . c (CO32- ) > c (HCO3- )
b. 2c (CO32- ) + c (HCO3- ) + c (OH- ) = c (H+ ) + c (Na+ )
c. c (H2CO3) + c (HCO3- ) + c (CO32- ) =0.2molL-1
��3����ҵ�Ͽ���CO2���Ƽ״�
��CO2 (g) + 3H2(g) ![]() CH3OH(g) + H2O(g) ��H < 0
CH3OH(g) + H2O(g) ��H < 0
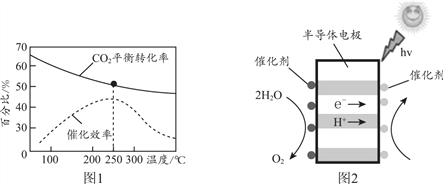
����ͼ1������ʵ�ʹ�ҵ�����У���Ӧ�¶�ѡ��250��������________��
�����ù���ԭ������CO2��H2O�Ʊ�CH3OH��װ����ͼ2��д���Ҳ�ĵ缫��Ӧʽ________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com