
| A. | 水中的氧气少了 | B. | 水中的亚硝酸盐浓度大了 | ||
| C. | 水中的钙、镁离子多了 | D. | 水中的CO2多了 |
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:实验题
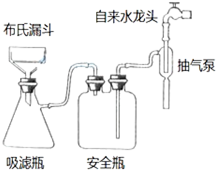 某学生预测定味精(味精的主要成分化学式为C5H8NO4Na•H2O)中食盐的含量,做了如下实验:
某学生预测定味精(味精的主要成分化学式为C5H8NO4Na•H2O)中食盐的含量,做了如下实验: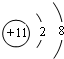 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阿司匹林有解热阵痛的作用 | |
| B. | 服用阿司匹林后出现肠胃道反应是中毒的表现,应立即停药 | |
| C. | 阿司匹林在干燥空气中不稳定,所以通常制成肠溶片 | |
| D. | 阿司匹林有治疗癌症的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将FeCl3固体放入水中搅拌 | |
| B. | 向FeCl3溶液中加入NaOH溶液 | |
| C. | 加热FeCl3溶液 | |
| D. | 向沸水中滴加饱和FeCl3溶液,并加热至红褐色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com