
【题目】如图装置(1)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为2K2S2+KI3![]() K2S4+3KI。装置(2)为电解池的示意图。当闭合开关K时,X附近溶液先变红,下列说法正确的是( )
K2S4+3KI。装置(2)为电解池的示意图。当闭合开关K时,X附近溶液先变红,下列说法正确的是( )

A.K+从右到左通过离子交换膜
B.电极M的反应式:I3﹣+2e﹣=3I﹣
C.电极X的反应式:4OH﹣﹣4e﹣═O2↑+2H2O
D.当电极Y有0.2mole﹣转移时,产生0.1molCl2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某化合物的分子式为![]() ,A属于第ⅥA族元素,B属于第ⅦA族元素,A和B在同一周期,它们的电负性分别为
,A属于第ⅥA族元素,B属于第ⅦA族元素,A和B在同一周期,它们的电负性分别为![]() 和
和![]() ,已知
,已知![]() 分子的键角为
分子的键角为![]() 。下列推断不正确的是
。下列推断不正确的是 ![]()
![]()
A.![]() 分子的空间构型为V形
分子的空间构型为V形
B.![]() 键为极性共价键,
键为极性共价键,![]() 分子为非极性分子
分子为非极性分子
C.![]() 分子中A原子采取
分子中A原子采取![]() 杂化
杂化
D.![]() 分子中无H原子,分子间不能形成氢键
分子中无H原子,分子间不能形成氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是
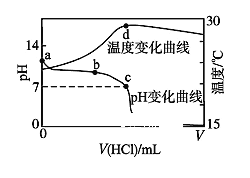
A. a点由水电离出的c(OH-)=1.0×10-14 mol·L-1
B. b点:c(NH4+)+c(NH3·H2O)=c(Cl-)
C. c点:c(Cl-)>c(NH4+)
D. d点:达到滴定终点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基于新材料及3D打印技术,科学家研制出一种微胶囊吸收剂能将工厂排放的CO2以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入Na2CO3溶液,其原理如图所示。
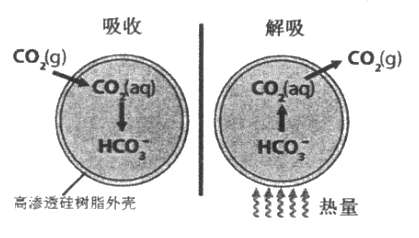
(1)这种微胶囊吸收CO2的原理是_____________(用离子方程式解释),此过程是_______(填“吸收”或“放出”)能量的过程。
(2)在吸收过程中关于胶囊内溶液下列说法正确的是_____________。
a.吸收前溶液中c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
b.吸收过程中,体系中所有的含碳微粒是CO32-、HCO3-、H2CO3
c.当n(CO2):n(Na2CO3)=1:3时,溶液中c(CO32-)<c(HCO3-)
d.溶液中始终有c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
(3)将吸收的CO2催化加氢可制得乙烯。
已知:2CO2(g)+6H2(g) ![]() C2H4(g)+4H2O(g)△H=-127.8 kJ/mol,如图曲线a表示在体积为2 L的恒容容器中,投料为1 mol CO2和3 mol H2时,测得温度对CO2的平衡转化率的影响,改变投料比测量后得到曲线b。
C2H4(g)+4H2O(g)△H=-127.8 kJ/mol,如图曲线a表示在体积为2 L的恒容容器中,投料为1 mol CO2和3 mol H2时,测得温度对CO2的平衡转化率的影响,改变投料比测量后得到曲线b。
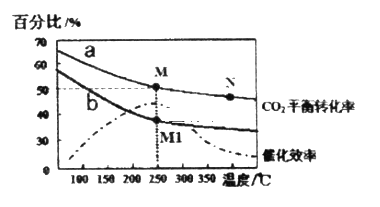
①根据曲线a计算250℃时该反应的化学平衡常数K=_____________(带入数值列出计算式即可)
②b条件下投料比n(H2)/n(CO2)______3(填“>”、“<”或“=”),判断依据是____________________________
③下列说法正确的是_____________。
a.平衡常数大小:M=M1> N
b.其他条件不变,b条件时增加催化剂用量,则250℃时CO2的平衡转化率可能达到M
c.当压强、混合气体的密度或n(H2)/n(CO2)不变时均可视为化学反应已达到平衡状态
d.工业生产中采取较高温度(250 ℃左右)是为了提高催化剂活性加快反应速率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如下图所示。下列说法错误的是
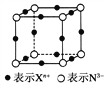
A. X元素的原子序数是19
B. Xn+中n=1
C. 该晶体中阳离子与阴离子个数比为3∶1
D. 晶体中每个N3-周围有6个等距离且最近的Xn+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出11种元素在周期表中的位置,按要求回答下列各题:

(1)这11种元素中,化学性质最不活泼的元素是______(填元素符号,下同),得电子能力最强的原子是______,失电子能力最强的单质与水反应的化学方程式__________。
(2)元素④的离子结构示意图为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.2-甲基丁烷也称异丁烷B.烷烃 的正确命名是2-甲基-3-丙基戊烷
的正确命名是2-甲基-3-丙基戊烷
C.C4H9Cl有3种同分异构体D.三元轴烯(![]() )与苯互为同分异构体
)与苯互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池的应用很广,其正极材料可再生利用。某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等。充电时,该锂离子电池负极发生的反应为6C+xLi++xe- = LixC6。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。

回答下列问题:
(1)LiCoO2中,Co元素的化合价为 。
(2)写出“正极碱浸”中发生反应的离子方程式 。
(3)“酸浸”一般在80℃下进行,写出该步骤中发生的所有氧化还原反应的化学方程式 ;可用盐酸代替H2SO4和H2O2的混合液,但缺点是 。
(4)写出“沉钴”过程中发生反应的化学方程式 。
(5)充放电过程中,发生LiCoO2与Li1-xCoO2之间的转化,写出放电时电池反应方程式 。
(6)上述工艺中,“放电处理”有利于锂在正极的回收,其原因是 。在整个回收工艺中,可回收到的金属化合物有 (填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com