
【题目】仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | … |
C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | … |
A. C6H14 B. C6H12 C. C7H12 D. C7H14
 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】某科研单位利用电化学原理用SO2来制备硫酸,装置如下图,含有某种催化剂。电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。
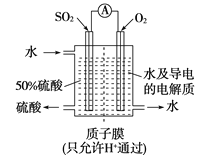
(1)通入SO2的电极为__________极,其电极反应式为_________________,此电极区pH_______(填“增大”“减小”或“不变”)。
(2)若通入SO2的速率为2.24 L/min(标准状况),为稳定持续生产,硫酸溶液的浓度应维持不变,则左侧水的流入速率是 (结果用 mL/min表示)
(3)以此电源电解足量的硝酸银溶液,若阴极产物的质量为21.6 g,则阳极产生气体标准状况下体积为__________L。
(4)常温时,BaSO4的Ksp=1.08×10-10。现将等体积的BaCl2溶液与3.5×10-3mol/L的Na2SO4溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为________。
(5)已知:Fe2O3(s)+3C(石墨)==2Fe(s)+3CO(g) ΔH =+489.0 kJ·mol-1
CO(g)+1/2O2(g)==CO2(g) ΔH=-283.0 kJ·mol-1
C(石墨)+O2(g)==CO2 (g) ΔH=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)==2Fe2O3(s)的ΔH为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】在研究金矿床物质组分的过程中,通过分析发现了Cu-Ni-Zn-Sn-Fe多金属互化物。
(1)某种金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于 (填“晶体”或“非晶体”),可通过 方法鉴别。
(2)基态Ni2+的核外电子排布式 ;配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于 晶体;Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO FeO(填“<”或“>”)。
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为 ;类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H—S—C≡N)的沸点低于异硫氰酸(H—N=C=S)的沸点,其原因是 ;写出一种与SCN—互为等电子体的分子 (用化学式表示)。
(4)氨基乙酸铜的分子结构如图,碳原子的杂化方式为 。
![]()
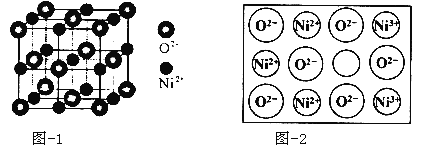
(5)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为apm,列式表示NiO晶体的密度为 g/cm3(不必计算出结果,阿伏加德罗常数的值为NA)。人工制备的NiO晶体中常存在缺陷(如图):一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。已知某氧化镍样品组成Ni0.96O,该晶体中Ni3+与Ni2+的离子个数之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属晶体的叙述正确的是
A.用铂金做首饰不能用金属键理论解释
B.固态和熔融时易导电,熔点在1000℃左右的晶体可能是金属晶体
C.Li、Na、K的熔点逐渐升高
D.金属导电和熔融电解质(或电解质溶液)导电的原理一样。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。

(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是_____________________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是____________________。再由a向c中加2 mL蒸馏水,c中的实验现象是 ___________________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是_____________。理由是_____________。
方案 | 反应物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将红热的固体单质甲放入显黄色的乙的浓溶液中,剧烈反应产生混合气体A,A在常温下不与空气作用,有如图变化关系:

(1)C的化学式为________。
(2)写出甲跟乙反应的化学方程式:______________________
(3)写出单质丙与乙的浓溶液反应的化学方程式:_________________
(4)写出单质丙与乙的稀溶液反应生成气体B的离子方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化钙在2973 K时熔化,而NaCl在1074 K时熔化,二者的离子间距和晶体结构都类似,有关它们熔点差别较大的原因叙述不正确的是
A.氧化钙晶体中阴、阳离子所带电荷数多
B.氧化钙晶格能比氯化钠的晶格能大
C.两种晶体的晶胞结构类型不同
D.氧化钙、氯化钠的离子间距类似情况下,晶格能主要由阴、阳离子所带电荷数决定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室使用的浓盐酸的溶质质量分数为36.5%,密度为1.19 g·cm-3,则该盐酸的物质的量浓度是( )
A.11.9 B.11.9 mol·L-1 C.0.012 mol·L-1 D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是 ( )
A. 丙烯性质与乙烯相似
B. 饱和一元羧酸的性质与乙酸相似
C. 苯与甲苯都能使酸性高锰酸钾溶液褪色
D. 所有醇都能与羧酸在一定条件下发生酯化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com