
| A. | 在强碱性溶液中:Na+、K+、[Al(OH)4]-、CO32- | |
| B. | 在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| C. | 在c(H+)=10-13mol•L-1的溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
分析 A.强碱溶液中该组离子之间不反应;
B.离子之间结合生成络离子;
C.c(H+)=10-13mol•L-1的溶液,显碱性;
D.pH=1的溶液,显酸性,离子之间发生氧化还原反应.
解答 解:A.强碱溶液中该组离子之间不反应,可大量共存,故A选;
B.Fe3+、SCN-结合生成络离子,不能共存,故B不选;
C.c(H+)=10-13mol•L-1的溶液,显碱性,碱性溶液中不能大量存在NH4+、Al3+,故C不选;
D.pH=1的溶液,显酸性,Fe2+、NO3-发生氧化还原反应,不能共存,故D不选;
故选A.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A | B | C | D |
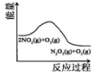 | 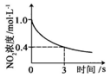 |  | 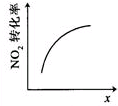 |
| 升高温度,平衡常数 减小 | 0~3s内,反应速率为v(NO2)=0.2mol•L-1•s-1 | t1时仅加入催化剂,平 衡向正方向移动 | 达平衡时,仅改变x, 则x为c(O2) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
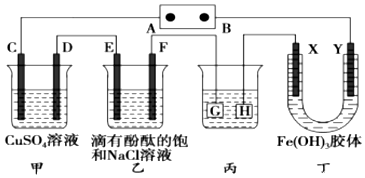
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,1 mol任何物质的体积都约为22.4 L | |
| B. | 在标准状况下,0.5 mol任何气体的体积都约为11.2 L | |
| C. | 在常温常压下,1 mol任何气体的体积都约为22.4 L | |
| D. | 在标准状况下,0.5 mol CCl4所占有的体积约为11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同密度、同压强的CO和C2H4 | B. | 同温度、同体积的O2和N2 | ||
| C. | 同体积、同密度的C2H4和N2 | D. | 同压强、同体积的O2和N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 称取2.0gNaOH固体 | 先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 |
| B | 配制MgCl2、AlCl3溶液中分别通入氨气 | 比较镁、铝的金属性强强弱 |
| C | 检验溶液中是否含有NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
| D | 向NaBr溶液中滴入少量的氯水和CCl2,振荡、静置,溶液下层呈橙红色 | Cl-的还原性强于Br- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com