
����Ŀ��������ͼ��ʾװ�òⶨ�к��ȵ�ʵ�鲽�����£�

������Ͳ��ȡ50mL0.50mol��L-1���ᵹ��С�ձ��У���������¶ȣ�������һ��Ͳ��ȡ50mL0.55mol��L-1NaOH��Һ��������һ�¶ȼƲ�����¶ȣ��۽�NaOH��Һ����С�ձ��У��跨ʹ֮��Ͼ��ȣ���û��Һ����¶ȣ��ش��������⣺
��1��Ϊʲô����NaOH��ҺҪ�Թ���____________________��
��2������NaOH��Һ����ȷ������________(�����)��
A���ز������������� B���������������� C��һ��Ѹ�ٵ���
��3��ʹ������NaOH��Һ��Ͼ��ȵ���ȷ������________(�����)��
A�����¶ȼ�С�Ľ���
B���ҿ�ӲֽƬ�ò���������
C����������ձ�
D���������¶ȼ��ϵĻ��β������������ؽ���
��4���ֽ�һ������ϡ����������Һ��ϡ����������Һ��ϡ��ˮ�ֱ��1L1mol��L-1��ϡ����ǡ����ȫ��Ӧ���䷴Ӧ�ȷֱ�Ϊ��H1����H2����H3�����H1����H2����H3�Ĵ�С��ϵΪ________��
��5��________(��ܡ����ܡ�)��Ba(OH)2��Һ�������������������Һ�����ᣬ������_____________��
���𰸡�ȷ�����ᱻ��ȫ�к� CD��H1����H2����H3����H2SO4��Ba(OH)2��Ӧ����BaSO4�����������Ȼ�Ӱ�췴Ӧ�ķ�Ӧ��
��������
��1��ʵ���У�����NaOH�Թ�����ԭ����ȷ�����������ᷴӦ��ȫ��
��2����������������Һʱ������һ����Ѹ�ٵĵ��룬Ŀ���Ǽ���������ɢʧ�����ּܷ��ε�������������Һ������ᵼ������ɢʧ��Ӱ��ⶨ������ʴ�ΪC��
��3��ʹ������NaOH��Һ��Ͼ��ȵ���ȷ���������ǣ��������¶ȼ��ϵĻ��β������������ؽ������¶ȼƲ����������裬�ҿ�ӲֽƬ�ò���������ᵼ��������ʧ����������ձ�����ʹҺ�彦�����ʴ�ΪD��
��4���к�����ǿ����ǿ��ϡ��Һ��ȫ��Ӧ����1molˮ�ų���������һ������ϡ����������Һ��ϡ����������Һ��1L 1molL-1��ϡ����ǡ����ȫ��Ӧ������ͬ��һˮ�ϰ���������ʣ����ڵ���ƽ�⣬������������ȵģ�ϡ��ˮ��1L 1molL-1��ϡ����ǡ����ȫ��Ӧ�ų����������٣������ڷ�Ӧ�ʱ��Ǹ�ֵ�����ԡ�H1����H2����H3��
��5��������Ba(OH)2��Һ��Ӧ��������ˮ�⣬��������BaSO4�������÷�Ӧ�е������Ȼ�Ӱ�췴Ӧ�ķ�Ӧ�ȣ����Բ�����Ba(OH)2��Һ���������NaOH��Һ��������к��ȡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϵΪԪ�����ڱ��еڢ�B�塢ԭ������Ϊ57��71��Ԫ�ء�
(1)��(Dy)�Ļ�̬ԭ�ӵ����Ų�ʽΪ[Xe]4f106s2��������(Dy)ԭ����Χ�����Ų�ͼ��_____��
(2)���³��������籵ͭ�������к���Cu3+����̬ʱCu3+�ĵ����Ų�ʽΪ_______________��
(3)�۲�����������ϵԪ�صĵ��������ݣ��ж����п�����ʾ+3�۵�Ԫ����_______(��Ԫ������)��
������ϵԪ�صĵ�����(��λ��kJ��mol-1)
Ԫ�� | I1 | I2 | I3 | I4 |
Yb(��) | 604 | 1217 | 4494 | 5014 |
Lu(��) | 532 | 1390 | 4111 | 4987 |
La(��) | 538 | 1067 | 1850 | 5419 |
Ce(��) | 527 | 1047 | 1949 | 3547 |
(4)Ԫ����(Ce)�����γ������(NH4)2[Ce(NO3)6]��
���������������Ԫ�أ��縺���ɴ�С��˳��Ϊ_______________(��Ԫ�ط��ű�ʾ)��
��Ԫ��AlҲ�����Ƴɼ��������̬�Ȼ������ӱ�ʾΪ(AlCl3)2��������Al ԭ���ӻ���ʽΪ________��������������ѧ��������______________(����ĸ)��
a.���Ӽ� b.���Լ� C���Ǽ��Լ� d.��λ��
(5)PrO2(��������)�ľ���ṹ��CaF2���ƣ���������ԭ��λ�����ĺͶ��㣬��PrO2(��������)�ľ�������______����ԭ�ӣ���֪��������Ϊa pm���ܶ�Ϊ��g��cm-3��NA=________ (�ú�a�����Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д��ȷ���ǣ� ��
A. �ƺ���ˮ��Ӧ��Na��2H2O===Na����2OH����H2��
B. �Ȼ����백ˮ��Ӧ��Al3����3OH��===Al(OH)3��
C. ����������������2Al��6H��===2Al3����3H2��
D. ����ϡ���ᷴӦ��2Fe��6H��===2Fe3����3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��A��B��C��D��E��ԭ��������������A��B��C�ĵ����ڳ����¶�����̬��Cԭ�������������ǵ��Ӳ�����3����C��Eλ��ͬ���塣1 mol DAx��������A2C��Ӧ����44.8 L����״����G���塣A��B�ĵ�������ΪG��T�����ܱ������г���һ������G��T��һ�������·�����ӦG+T��W��δ��ƽ������ø����ʵ�Ũ�������ʾ��
���� | T | G | W |
10 minʱ��c/(mol/L) | 0.5 | 0.8 | 0.2 |
20 minʱ��c/(mol/L) | 0.3 | 0.2 | 0.6 |
�ش��������⣺
��1��A��B��C����ɼȺ����Ӽ��ֺ����ۼ��Ļ�����û�����Ļ�ѧʽΪ_________��
��2��B��C��D��E�ļ������У����Ӱ뾶�ɴ�С����Ϊ__________�������ӷ��ű�ʾ����
��3��J��L����A��B��C��E����Ԫ����ɵ����ֳ�����ʽ�Σ�J��L��Ͽɲ����д̼�����ζ�����壬д����������Һ������Ӧ�����ӷ���ʽ__________��J��L����ʹ���Ը��������Һ��ɫ����_______���ѧʽ����
��4��B2A4C2����ȼ�ϵ�طŵ�Ч�ʸߡ��õ�طŵ�ʱ����B2��A2C��������ӦʽΪ________����ع���һ��ʱ��������Һ��pH_____����������������С����������������
��5����A��B��C��D����Ԫ����ɵĵ��ʡ���������һ�������µ�ת����ϵ�����������Ͳ�����ʡ�ԣ���ͼ��ʾ����֪M���¡�
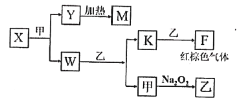
��X�ĵ���ʽΪ______��
����֪W���ҷ�Ӧ����K�ͼ���ij��Ҫ������������֮һ������䷴Ӧ���ʵķ���������Ӧ��Ũ�ȡ�����ѹǿ�⣬����______��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӫ�������У���������ˮ�ⷴӦ���ǣ� ��
A.����B.������C.������D.ֲ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݱ����Զ�����̼Ϊԭ�ϲ�������ĵ缫���ǿ���ԵĶ�����̼ˮ��Һ�ɵõ�����ȼ�ϣ���ԭ����ͼ��ʾ����װ�ù���ʱ�����������������
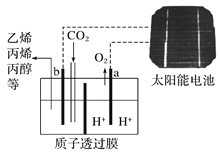
A. b����������ϩ�ĵ缫��ӦʽΪ��2CO2��12H����12e��===C2H4��4H2O
B. a��̫���ܵ�ص�����
C. a���Ϸ�����ԭ��Ӧ���ɱ����22.4 L����ʱ����·��ת�Ƶĵ�����Ϊ4NA
D. ��Һ��H��ͨ��������Ĥ��b���ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��mA(g)+nB(g) ![]() pC(g)+qQ(g)��m��n��p��qΪ��������ʱ���ﵽƽ��ı�־�ǣ��� ��
pC(g)+qQ(g)��m��n��p��qΪ��������ʱ���ﵽƽ��ı�־�ǣ��� ��
����ϵ��ѹǿ���ٸı� ����ϵ���¶Ȳ��ٸı� �۸���ֵ�Ũ�Ȳ��ٸı� �ܸ���ֵ������������ٸı�ݷ�Ӧ����VA:VB:VC:VD=m:n:p:q ��λʱ����m mol A�ϼ���Ӧ��ͬʱp mol CҲ�ϼ���Ӧ
A. �ۢܢݢ� B. �ڢۢܢ� C. �٢ۢܢ� D. �٢ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Na2O2����������ȷ����(����)
A��1 mol Na2O2������CO2��Ӧת�Ƶĵ���Ϊ1 mol
B����10 g H2��CO�Ļ��������ȼ�գ���������(H2O��CO2)ͨ��������Na2O2�����г�ַ�Ӧ����������Ϊ10 g
C����Na2O2Ͷ��FeSO4��Һ�����ɺ��ɫ����
D���������ʵ�����NaHCO3��Na2O2��Ϻ����ܱ������г�ּ����ų������ʣ�����ΪNa2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�����˶���ʹ�õĻ�������ܴ����Դ�ڱ����ȼ�գ�������һ��������ȼ�ϡ��Իش��������⣺
����ͼ��һ����������ȫȼ������CO2��1 mol H2O�����е������仯ͼ������ͼ�е���������������������������
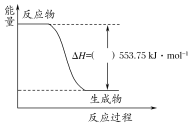
��д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ��____________________________________________��
(2)2SO2��g��+O2��g��![]() 2SO3��g����Ӧ���̵������仯��ͼ��ʾ����֪1 mol SO2��g������Ϊ1 mol SO3��g������H=��99 kJmol-1��
2SO3��g����Ӧ���̵������仯��ͼ��ʾ����֪1 mol SO2��g������Ϊ1 mol SO3��g������H=��99 kJmol-1��
��ش��������⣺
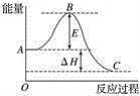
��ͼ����H=______kJmol-1��
����֪�������ȼ����Ϊ296 kJmol-1��������S��s������1 mol SO3��g������H=______ kJmol-1��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com