

分析 装置A中硫酸与磷矿反应,操作a是把固体与液体分开,应为过滤,装置B中氨气与磷酸反应,操作b是由溶液中析出晶体,应经过蒸发浓缩、冷却结晶等操作得到磷铵,磷酸受热容易分解,在结晶时应采用低温蒸发结晶.磷石膏中含有硫酸钙,经过煅烧生成水泥,得到二氧化硫窑气,净化后得二氧化硫,在接触室中氧化得三氧化硫,与水反应得硫酸,可以再参加与磷矿石的反应,尾气中二氧化硫循环利用.
(1)未净化的SO2气体中有粉尘等杂质,可以使催化剂中毒;
(2)操作b是从溶液中获得晶体;
(3)增大SO3与吸收剂的接触面积;
(4)预热进入接触室的反应混合气体,及时将反应放出的热量吸收;400℃~500℃、101KPa时二氧化硫的转化率已经很高,再增大压强,会增大成本,二氧化硫转化率提高不大;
(5)SO2、微量的SO3和酸雾都能与碱反应,不能利用碱测定,SO2具有还原性,可以利用强氧化剂测定;
(6)由上述分析可知,硫酸、二氧化硫可以循环利用;
(7)磷铵是一种常用复合肥,经分析其中氮与磷原子数之比为3:2,磷铵的化学式可以表示为:(NH4)3H3(PO4)2,根据P元素守恒可得关系式:2P~(NH4)3H3(PO4)2,根据关系式计算.
解答 解:装置A中硫酸与磷矿反应,操作a是把固体与液体分开,应为过滤,装置B中氨气与磷酸反应,操作b是由溶液中析出晶体,应经过蒸发浓缩、冷却结晶等操作得到磷铵,磷酸受热容易分解,在结晶时应采用低温蒸发结晶.磷石膏中含有硫酸钙,经过煅烧生成水泥,得到二氧化硫窑气,净化后得二氧化硫,在接触室中氧化得三氧化硫,与水反应得硫酸,可以再参加与磷矿石的反应,尾气中二氧化硫循环利用.
(1)未净化的SO2气体中有粉尘等杂质,可以使催化剂中毒,
故答案为:防止接触室中的催化剂中毒;
(2)操作b是从溶液中获得晶体,从溶液中析出晶体的方法是:将溶液蒸发浓缩、冷却结晶可得相应晶体,
故答案为:蒸发浓缩、冷却结晶;
(3)吸收塔内安装有许多瓷环,增大SO3与吸收剂的接触面积,使SO3充分吸收,
故答案为:增大SO3与吸收剂的接触面积,使SO3充分吸收;
(4)接触室内安装热交换器,可以预热进入接触室的反应混合气体,及时将反应放出的热量吸收,防止接触室温度偏高,400℃~500℃、101KPa时二氧化硫的转化率已经很高,再增大压强,会增大成本,二氧化硫转化率提高不大,该温度下反应速率较快、催化剂活性最好,
故答案为:预热进入接触室的反应混合气体,及时将反应放出的热量吸收,防止接触室温度偏高;400℃~500℃、101KPa;
(5)A.NaOH溶液与SO2、微量的SO3和酸雾反应,测量的SO2含量偏高,故A错误;
B.硫酸尾气中只有SO2能被酸性KMnO4溶液氧化,溶液颜色由紫红色变为无色,根据KMnO4溶液的体积结合方程式计算SO2的含量,故B正确;
C.氨水与SO2、微量的SO3和酸雾反应,测量的SO2含量偏高,故C错误;
D.硫酸尾气中只有SO2能被碘水氧化SO2,溶液颜色由蓝色变为无色,根据碘水溶液的体积结合方程式计算SO2的含量,故D正确,
故答案为:BD;
(6)由上述分析可知,H2SO4、SO2可以循环利用,
故答案为:H2SO4、SO2;
(7)磷铵是一种常用复合肥,经分析其中氮与磷原子数之比为3:2,磷铵的化学式可以表示为:(NH4)3H3(PO4)2,设需要磷矿y吨,则:
2P~~~~~~~(NH4)3H3(PO4)2
62 247
y吨×80%×$\frac{31×2}{310}$×(1-7%) 74.1吨
所以62:244=y吨×80%×$\frac{31×2}{310}$×(1-7%):74.1吨
解得:y=125
故答案为:125.
点评 本题考查物质的分离与提纯方法的综合应用,题目难度中等,涉及物质的分离提纯、对条件的控制、对装置与原理的分析评价、实验方案设计、化学计算等,(7)中计算为易错点、难点,关键根据原子数目之比确定磷铵的组成,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 将二氧化硫气体通入紫色石蕊试液中,观察溶液颜色变化 | 证明二氧化硫具有漂白性 |
| B | 向2mL 1mol•L-1NaOH溶液中先加入3滴1mol•L-1 FeCl3,再加入3滴1mol•L-1MgCl2溶液 | 证明K[Mg(OH)2]>K[Fe(OH)3] |
| C | 相同条件下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2分解速率的影响 |
| D | 向2mL品红溶液和2mL加入少许醋酸的品红溶液中分别滴入3滴NaClO的84消毒液,观察红色褪色的快慢 | 证明溶液pH的减少,84消毒液的氧化能力增强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7种 | B. | 6种 | C. | 5种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
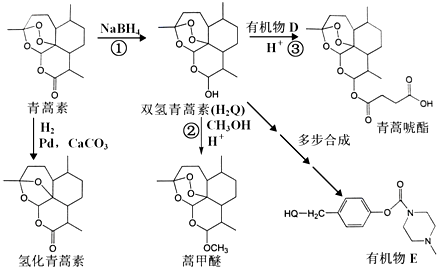
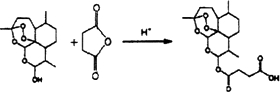 .
.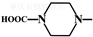 外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式
外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式 ,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有3种.
,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有3种.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.
草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| 取少量黑色固体,加入适量稀盐酸或稀硫酸, 在溶液中加入硫氰化钾溶液 | 溶液不变红色,则假设一成立, 溶液变成红色,则假设一不成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaHCO3溶液中通CO2至pH=7:c(Na+)=c(HCO3-)+2c(CO32-) | |
| B. | 向CH3COONa溶液中加入等浓度等体积的盐酸:c(Na+)=c(Cl-) | |
| C. | 向NaHSO4溶液中加入等浓度等体积的Ba(OH)2溶液:pH=13 | |
| D. | 向氨水中加入少量NH4Cl固体:$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 焰火的五彩缤纷是某些金属元素化学性质的体现 | |
| B. | 高纯度的单晶硅用于制造登月车的光电池和光导纤维 | |
| C. | 可溶性铜盐有毒,但在生命体中,铜是一种不可缺少的微量元素 | |
| D. | 用明矾可以将自来水净化成纯净水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com