
【题目】雾霾天气是一种大气污染状态,雾霾的源头多种多样,比如汽车尾气、工业排放、建筑扬尘、垃圾焚烧,甚至火山喷发等。
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化。
①已知部分化学键的键能如下

请完成汽车尾气净化中NO(g)和CO(g)发生反应的热化学方程式
2NO(g)+2CO( g) ![]() N2( g)+2CO2(g) △H=___________kJ·mol—1
N2( g)+2CO2(g) △H=___________kJ·mol—1
②若上述反应在恒温、恒容的密闭体系中进行,并在t1时刻达到平衡状态,则下列示意图符合题意的是 ___(填选项序号)。(下图中V正、K、n、P总分别表示正反应速率、平衡常数、物质的量和总压强)

(2)在t1℃下,向体积为10 L的恒容密闭容器中通入NO和CO,测得不同时间NO和CO的物质的量如下表:

t1℃时该反应的平衡常数K= _______,既能增大反应速率又能使平衡正向移动的措施是
____。(写出一种即可)
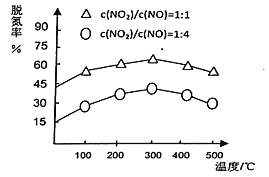
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。在氨气足量的情况下,不同c(NO2)/C(NO)、不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请回答温度对脱氮率的影响____________________,给出合理的解释:____________________。
【答案】 -538 D 500 加压 300℃之前,温度升高脱氮率逐渐增大;300℃之后,温度升高脱氮率逐渐减小 300℃之前,反应未平衡,反应向右进行,脱氮率增大;300℃时反应达平衡,后升温平衡逆向移动,脱氮率减小
【解析】(1)①化学反应的焓变等于反应物旧键断裂吸收的能量和生成物中新键形成释放的能量之差,所以2NO(g)+2CO(g)![]() N2(g)+2CO2(g)的△H=(2×632+1072×2)-(750×4+946)kJ/mol=-538kJ/mol;②A、t1时正反应速率仍然在变化,说明没有达到平衡状态,选项A错误;B、平衡常数只受温度的影响,反应在恒温、恒容的密闭体系中进行,K始终不变,选项B错误;C、t1时二氧化碳和一氧化氮的物质的量相等但还在变化,说明正逆反应速率不相等,反应没有达到平衡状态,选项C错误;D、该反应正反应为气体体积缩小的反应,当反应前后气体总压不变时,则反应达到了平衡状态,选项D正确;答案选D;
N2(g)+2CO2(g)的△H=(2×632+1072×2)-(750×4+946)kJ/mol=-538kJ/mol;②A、t1时正反应速率仍然在变化,说明没有达到平衡状态,选项A错误;B、平衡常数只受温度的影响,反应在恒温、恒容的密闭体系中进行,K始终不变,选项B错误;C、t1时二氧化碳和一氧化氮的物质的量相等但还在变化,说明正逆反应速率不相等,反应没有达到平衡状态,选项C错误;D、该反应正反应为气体体积缩小的反应,当反应前后气体总压不变时,则反应达到了平衡状态,选项D正确;答案选D;
(2)NO和CO反应生成CO2和N2,反应方程式为:
2NO + 2CO ![]() 2CO2 + N2
2CO2 + N2
起始浓度:1×l0-2 3.6×l0-2 0 0
转化浓度:0.9×l0-2 0.9×l0-2 0.9×l0-2 0.45×l0-2
平衡浓度:0.1×l0-2 2.7×l0-2 0.9×l0-2 0.45×l0-2
反应的平衡常数K= ![]() =500,加压既能增大反应速率又能使平衡正向移动,故采取的措施是加压;(3)根据图示信息得到:①300℃之前,温度升高脱氮率逐渐增大;300℃之后,温度升高脱氮率逐渐减小,②这是因为:300℃之前,反应未平衡,反应向右进行,脱氮率增大;300℃时反应达平衡,后升温平衡逆向移动,脱氮率减小。
=500,加压既能增大反应速率又能使平衡正向移动,故采取的措施是加压;(3)根据图示信息得到:①300℃之前,温度升高脱氮率逐渐增大;300℃之后,温度升高脱氮率逐渐减小,②这是因为:300℃之前,反应未平衡,反应向右进行,脱氮率增大;300℃时反应达平衡,后升温平衡逆向移动,脱氮率减小。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图1是部分短周期元素的常见化合价与原子序数的关系图: 
(1)元素F在周期表中的位置 .
(2)C与D形成原子个数比为1:1的化合物中所含化学键类型为 .
(3)C、D、G对应的简单离子半径由大到小顺序是 . (用离子符号回答)
(4)某同学设计实验装置如图2,证明A、B、F的非金属性强弱关系:
①溶液a和溶液b分别为 , .
②溶液c中的离子反应方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2Fe+3Br2=2FeBr3,Fe2+的还原性大于Br-。现有16.8 g铁和0.3 mol Br2反应后加入水得到澄清溶液后,通入a mol Cl2。则下列叙述不正确的是
A. 当a=0.1时,发生的反应为2Fe2++Cl2=2Fe3++2Cl-
B. 当a=0.45时,发生的反应为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
C. 若溶液中Br-有一半被氧化时,c(Fe3+)∶c(Br-)∶c(Cl-)=1∶1∶3
D. 当0<a<0.15时,始终有2c(Fe2+)+3c(Fe3+)+c(H+)=c(Cl-)+c(Br-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,0.01mol·L-1的NaOH溶液中由水电离生成的H+浓度( )
A.0.01mol·L-1B.1×10-7mol·L-1C.1×10-12mol·L-1D.1×10-14mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一容积不变的密闭容器中充入一定量A和B,发生如下反应:x A(g)+2B(s)![]() y C(g);△H <0。在一定条件下,容器中 A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
y C(g);△H <0。在一定条件下,容器中 A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
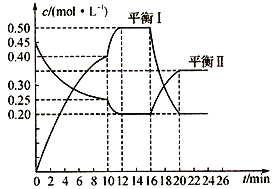
(1)用A的浓度变化表示该反应0~10min内的平均反应速率v(A)=______________;
(2)根据图示可确定x:y=______________;
(3)0~l0min容器内压强______________(填“变大”,“不变”或“变小”)
(4)推测第l0min引起曲线变化的反应条件可能是______________(填序号);第16min引起曲线变化的反应条件可能是______________(填序号);
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废电池必须进行集中处理的问题被提到议事日程。其首要原因是( )
A.防止汞、镉和铅等重金属离子对土壤和水源的污染
B.为了利用电池外壳的金属材料
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中的石墨电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液,按pH由小到大顺序排列的是( )
①0.1mol/L HCl溶液②0.1mol/L H2SO4溶液③0.1mol/L NaOH溶液④0.1mol/L CH3COOH溶液
A.①②④③B.②①④③C.③④①②D.④③②①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com