
25℃时,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示。下列说法正确的是
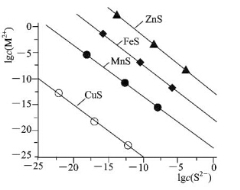
A.Ksp(CuS)约为l×10-20
B.向Cu2+浓度为10-5mol?L-1废水中加入ZnS粉末,会有CuS沉淀析出
C.向l00mL浓度均为10-5mol?L-1 Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol?L-1 Na2S溶液,Zn2+先沉淀
D.Na2S溶液中:2c(S2-)+2c(HS-)+2c(H2S)=c(Na+)
BD
【解析】
试题分析:A、根据题给图像知,Ksp(CuS)约为l×10-10,错误;B、根据题给图像知,Ksp(CuS) <Ksp(ZnS),向Cu2+浓度为10-5mol?L-1废水中加入ZnS粉末,会有CuS沉淀析出,正确;C.根据题给图像知,Ksp(CuS) <Ksp(FeS)<Ksp(ZnS),向l00mL浓度均为10-5mol?L-1 Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol?L-1 Na2S溶液,Cu2+先沉淀,错误;D、根据物料守恒知Na2S溶液中:
2c(S2-)+2c(HS-)+2c(H2S)=c(Na+),正确。
考点:考查沉淀溶解平衡,物料守恒式。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
9.2 g金属钠投入到足量的重水(2H216O)中,则产生的气体中含有
A.0.2 mol中子 B.0.4 mol电子
C.0.2 mol质子 D.0.4 mol分子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:选择题
化学与社会、生活密切相关,下列说法不正确的是
A.在食品袋中放入盛有CaO和硫酸亚铁的透气小袋,可防止食物受潮、氧化变质
B.MgO、Al2O3的熔点很高,工业上用于制作耐高温材料,也用与冶炼铝和镁
C.发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
D.利用ClO2对自来水消毒主要是因为ClO2具有强氧化性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,11.2 L NO和11.2 L SO3的分子总数为0.5NA
B.0.1molBr2与足量H2O或NaOH反应转移的电子数均为0.1NA
C.0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价键数均为0.4NA
D.在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:填空题
(14分)二氧化碳的捕集、利用与封存(CCUS)是我国能源领域的一个重要战略方向,CCUS或许发展成一项重要的新兴产业。
(1)国外学者提出的由CO2制取C的太阳能工艺如图所示

①“热分解系统”发生的反应为2Fe3O4 6FeO+O2↑,每分解lmolFe3O4转移电子的物质的量为 。
6FeO+O2↑,每分解lmolFe3O4转移电子的物质的量为 。
②“重整系统”发生反应的化学方程式为 。
(2)二氧化碳催化加氢合成低碳烯烃是目前研究的热门课题,起始时以0.1MPa,n(H2):n(CO2)=3:1的投料比充入反应器中,发生反应:2CO2(g)+6H2(g)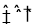 C2H4(g)+4H2O(g)△H,不同温度下平衡时的四种气态物质的物质的量如图所示:
C2H4(g)+4H2O(g)△H,不同温度下平衡时的四种气态物质的物质的量如图所示:

①曲线b表示的物质为 (写化学式)。
②该反应的△H 0(填:“>” 或“<”)
③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是 (列举l项)。
(3)据报道以二氧化碳为原料采用特殊的电极电解强酸性的二氧化碳水溶液可得到多种燃料,其原理如图所示。

①该工艺中能量转化方式主要有 (写出其中两种形式即可)。
②电解时其中b极上生成乙烯的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:选择题
己知:
①2H2(g)+O2(g) 2H2O(g)△H1
2H2O(g)△H1
②H2(g)+Cl2(g) 2HCl(g)△H2
2HCl(g)△H2
③4H Cl (g)+O2(g) 2 Cl2(g)+2H2O(g)△H3
2 Cl2(g)+2H2O(g)△H3
④N2(g)+3H2(g) 2NH3(g)△H4
2NH3(g)△H4
⑤2NH3(g)+3 Cl2(g) N2(g)+6HCl(g)△H5
N2(g)+6HCl(g)△H5
下列关于上述反应焓变的判断正确的是
A.△H1>0,△H2>0 B.△H3>0,△H4>0
C.△H2=△H4+△H5 D.△H3=△H1-2△H2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:选择题
25℃时,下列各组离子在指定溶液中一定能大量共存的是
A.滴入石蕊试液显蓝色的溶液中:K+、Na-、HSO3-、ClO-
B.0.1mol?L-l的Fe(NO3)2溶液中:Na+、H+、SCN-、I-
C.0.1mol?L-l的NaAlO2溶液中:K+、H+、NO3-、SO42-
D.由水电离产生的c(H+)=1×10-13mol?L-l的溶液中:Na+、Ba2+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:选择题
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
选项 | 甲 | 乙 | 丙 |
A | AlCl3 | NH3·H2O | NaAlO2 |
B | NaOH | (NH4)2SO3 | H2SO4 |
C | SiO2 | NaOH | HF |
D | CO2 | Ca(OH)2 | Na2CO3(aq) |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省深圳市高三第一次调研考试理综化学试卷(解析版) 题型:实验题
(16分)甲、乙组同学分别做了以下探究实验。
(1)甲组探究Cl2与Na2SO3溶液反应,实验装置如下。
①请指出该装置的不足之处 、 。

②Cl2与Na2SO3溶液反应的离子方程式为 。
③设计实验,简述实验步骤,证明洗气瓶中的Na2SO3已被氧化 。
乙组探究乙酸乙酯(沸点77.1℃)在不同温度、不同浓度NaOH溶液中的水解速率。
取四支大小相同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加热相同时间后,记录酯层的体积来确定水解反应的速率。

④请完成上表,其中V2 = ,V4 = ,V5 = 。
⑤实验中,可用饱和食盐水替代蒸馏水,其优点是 ;但不能用饱和Na2CO3溶液替代蒸馏水,其原因是 。
⑥实验中,试管Ⅳ比试管Ⅱ中的酯层减少更快,其原因有:温度高速率快,还可能有 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com