
设NA为阿伏加德罗常数,下列说法正确的是( )
|
| A. | 2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
|
| B. | 32g氧气所含原子数目为NA |
|
| C. | 17g氨气所含电子数目为10NA |
|
| D. | 1.8g水所含的质子数目为10NA |
考点:
阿伏加德罗常数.
专题:
阿伏加德罗常数和阿伏加德罗定律.
分析:
A、依据镁原子的结构分析;
B、从氧气是双原子分子分析计算;
C、从分子物质的量求算微粒数目;
D、依据分子物质的量和分子中质子数计算质子总数.
解答:
解:A、镁原子最外层电子数为2,2.4g金属镁变成镁离子时失去的电子数目为0.2NA,故A错误;
B、32g氧气的物质的量为1mol,1mol氧气所含原子数为2mol,故B错误;
C、17g氨气物质的量为1mol,1molNH3分子中含有电子数10mol,故C正确;
D、1.8g水物质的量为0.1mol,所含质子数为1mol,即NA,故D错误;
故选C.
点评:
本题考查了阿伏伽德罗常数的应用,明确微粒中的电子数、质子数、得失电子数的计算即可解答.


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是
①中实验②中现象()
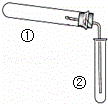
A. 铁粉与水蒸气加热 肥皂水冒泡
B. 加热NH4Cl和Ca(OH)2混合物 酚酞溶液变红
C. NaHCO3固体受热分解 澄清石灰水变浑浊
D. 石蜡油在碎瓷片上受热分解 Br2的CCl4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中溶质的物质的量浓度为1mol•L﹣1的是( )
-A.-将58.5 g NaCl溶解于1 L水中配成的溶液
-B.-含K+为2 mol的K2SO4溶液
-C.-将0.5 mol•L﹣1的NaNO3溶液100 mL加热蒸发掉50 g水的溶液
-D.-将250 g 胆矾溶于水并配成1 L溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
化学实验要注意安全,下列行为符合安全要求的是( )
|
| A. | 汽油着火时,立即用水灭火 |
|
| B. | 稀释浓硫酸时,将水倒入浓硫酸中 |
|
| C. | 浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
|
| D. | 浓硫酸溅到皮肤上,立即用稀NaOH溶液洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各物质所含原子数目,按由大到小顺序排列的是( )
①0.5mol NH3 ②标准状况下22.4L氦气 ③4℃9mL水 ④0.2mol H3PO4.
|
| A. | ①④③② | B. | ④③②① | C. | ②③④① | D. | ①④②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
配制250mL0.5mol/L的盐酸溶液,需4mol/L的盐酸的体积是( )
|
| A. | 25mL | B. | 31.3mL | C. | 12.5mL | D. | 100mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)0.25molH3PO4分子中含有氢原子的物质的量是 ,含有氧原子数目为 .
(2)0.3molH2O与0.4molCO2的物质的量之比为 ,所含分子数目之比为 ,所含氧原子数目之比为 .
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl﹣,则ACl2的摩尔质量是 ,A的相对原子质量是 ,ACl2的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列说法正确的是( )
|
| A. | 2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
|
| B. | 32g氧气所含原子数目为NA |
|
| C. | 17g氨气所含电子数目为10NA |
|
| D. | 1.8g水所含的质子数目为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的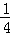 .
.
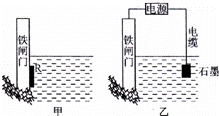
(1)为了降低某水库的铁闸门被腐蚀的速率,可以采用如图所示甲的方案,属于 原理(填“原电池”或“电解池”)
(2)图中乙方案也可降低铁闸门腐蚀速率,称为 保护法.
(3)将5mol/L CuSO4溶液200mL用惰性电极电解一段时间后,从其中的一个电极收集到标准状况下448mL气体,为使电解后的溶液恢复到开始的浓度,应向电解后的溶液中加入 物质(填化学式).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com