

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
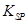 = 2.70×10-39]
= 2.70×10-39] ZnS(aq)=Zn2++S2- CuS(s)
ZnS(aq)=Zn2++S2- CuS(s) CuS(aq)=Cu2++S2-,当c(H+)增大的情况下,c(S2-)减小的情况下,前者平衡正向移动,即离子积c(Zn2+)×c(S2-)小于Ksp(ZnS),并且离子积c(Cu2+)×c(S2-)大于Ksp(CuS),则Ksp(ZnS)较大
CuS(aq)=Cu2++S2-,当c(H+)增大的情况下,c(S2-)减小的情况下,前者平衡正向移动,即离子积c(Zn2+)×c(S2-)小于Ksp(ZnS),并且离子积c(Cu2+)×c(S2-)大于Ksp(CuS),则Ksp(ZnS)较大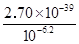 =2.7×10-20.4mol/L
=2.7×10-20.4mol/L

 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源:不详 题型:实验题
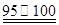 ℃CCl4+S2Cl2;② 2S+Cl2
℃CCl4+S2Cl2;② 2S+Cl2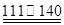 ℃S2Cl2。
℃S2Cl2。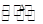 2SCl2。
2SCl2。
| 物质 | 沸点/℃ | 熔点/℃ |
| S | 445 | 113 |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
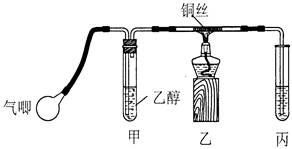
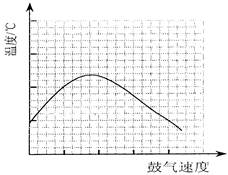
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
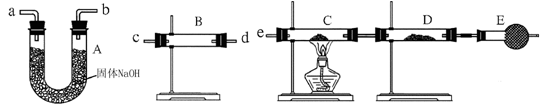
| 装置 | 所盛药品 | 实验现象 | 结论 |
| B | | | |
| C | CuO固体 | | |
| D | 无水CuSO4 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
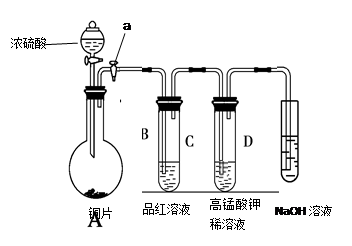
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | | 有白色沉淀生成,证明待测液中含SO42-。 |
| 步骤② | | |
| 步骤③ | | |
| …… | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 l3溶液溶解Ag的反应更快更完全,请解释其原因:
l3溶液溶解Ag的反应更快更完全,请解释其原因: | 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① ② …… | 若银镜消失,假设2成立。 若银镜不消失,假设2不成立。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 名称 | 乙二酸 | 乙二酸晶体 |
| 分子式 | H2C2O4 | H2C2O4·2H2O |
| 颜色状态 | 无色固体 | 无色晶体 |
| 溶解度(g) | 8.6(20℃) | — |
| 熔点(℃) | 189.5 | 101.5 |
| 密度(g·cm-3) | 1.900 | 1.650 |
 华,157℃时大量升华,并开始分解。草酸钙不溶于水。根据上述材料提供的信息,回答下列问题:
华,157℃时大量升华,并开始分解。草酸钙不溶于水。根据上述材料提供的信息,回答下列问题: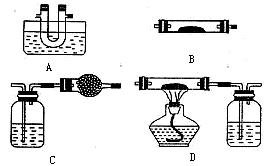
| A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色 |
| B.测定相同浓度的草酸和硫酸溶液的pH |
| C.测定草酸钠(Na2C2O4)溶液的pH |
| D.将草酸溶液加入Na2CO3溶液中,有CO2放出 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com