
科目:高中化学 来源: 题型:
 H2CO3+OH-
H2CO3+OH- H2CO3+OH-
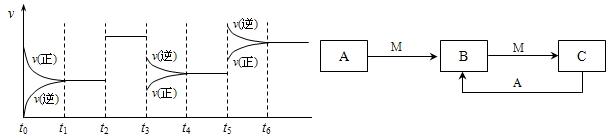
H2CO3+OH- 2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是
2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是 2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m.
2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m. 查看答案和解析>>
科目:高中化学 来源: 题型:
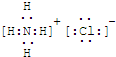
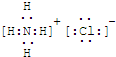
查看答案和解析>>
科目:高中化学 来源: 题型:
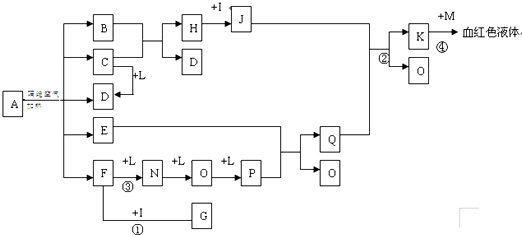
已知A为一无机盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反
应①常用于气体F的检验。
(1)写出G的电子式_______________,M的化学式_____________;
(2)写出反应②的离子反应方程式______________________________;
(3)写出反应③的化学反应方程式_____________;反应①—④中属于非氧化还原反应的是 ;
(4)用石墨电极电解溶液K时,电解初始阶段电极反应方程式为:
阴极___________________阳极___________________;
(5)已知A在隔绝空气条件下分解产生的各产物的物质的量之比为
B:C:D:E:F=1:2:2:2:2,写出A分解的反应方程式______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)用A~M分别代表一种物质,它们之间的转化关系如下图所示(部分生成物略去)。其中A为紫色晶体,B、H、J均为常见的单质气体,单质E在浓硝酸中钝化。
请回答下列问题:
(1)D的化学式是 ,L由3种元素组成,其电子式是 。
(2)E元素在周期表中的位置是 。工业上可利用C与E在高温下反应冶炼金属,该反应的化学方程式是 。
(3)用C与F溶液制H气体时,发生反应的化学方程式是 。
(4)用石墨电极电解D的水溶液时,阳极的电极反应式是 。
(5)在500 mL 0.2 mol/L K物质的水溶液中逐滴加入F的水溶液并不断搅拌,溶液中析出沉淀的质量发生变化,在右图中画出沉淀质量随加入F的物质的量的变化曲线。
查看答案和解析>>
科目:高中化学 来源:2011届辽宁省锦州市高三检测二(理综)化学部分 题型:填空题
已知A为一无机盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反
应①常用于气体F的检验。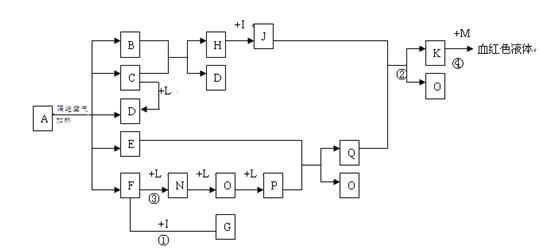
(1)写出G的电子式_______________,M的化学式_____________;
(2)写出反应②的离子反应方程式______________________________;
(3)写出反应③的化学反应方程式_____________;反应①—④中属于非氧化还原反应的是 ;
(4)用石墨电极电解溶液K时,电解初始阶段电极反应方程式为:
阴极___________________阳极___________________;
(5)已知A在隔绝空气条件下分解产生的各产物的物质的量之比为
B:C:D:E:F=1:2:2:2:2,写出A分解的反应方程式______________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com