
| A. | 同主族金属元素的原子半径越大,熔点越高 | |
| B. | 离子晶体固态或熔融状态下都能导电 | |
| C. | 原子最外层有3个电子的元素一定是主族元素 | |
| D. | 温度越高,金属晶体的导电性越好 |
分析 A.同主族金属性从上到下逐渐增强,金属键减弱;
B、离子晶体的构成微粒是阴、阳离子,要导电离子必须自由移动;
C、最外层有3个电子的原子是ⅢA族元素;
D、温度升高,金属导体的电阻增大.
解答 解:A.同主族金属性从上到下逐渐增强,金属键减弱,故同主族金属元素的原子半径越大熔点越低,故A错误;
B、离子晶体的构成微粒是阴、阳离子,要导电离子必须自由移动,离子晶体在固态时不能自由移动,所以离子晶体固态时不导电,故B错误;
C、最外层有3个电子的原子是ⅢA族元素,则一定为主族元素,故C正确;
D、温度升高,金属导体的电阻增大,导电性减小,故D错误;
故选C.
点评 本题考查主族元素的判断、元素周期律和导电性的问题,为高频考点,把握原子结构与元素的位置为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 100mL2mol•L-1NH4NO3溶液 | B. | 40mL0.5mol•L-1Ca(NO3)2溶液混合 | ||
| C. | 50mLl.5mol•L-1Al(NO3)3溶液 | D. | 150mL1mol•L-1Mg(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的强 | |
| D. | W的单质可用于制造光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 →CH≡C-CH═CH2
→CH≡C-CH═CH2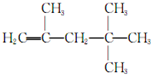 ,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的.在此反应中除生成甲外,同时还得到另一种产量更多的有机物丙,其最长的碳链仍为5个碳原子,丙是甲的同分异构体.则乙的结构简式是
,它是由不饱和烃乙的两个分子在一定条件下自身加成而得到的.在此反应中除生成甲外,同时还得到另一种产量更多的有机物丙,其最长的碳链仍为5个碳原子,丙是甲的同分异构体.则乙的结构简式是 ,丙的结构简式是
,丙的结构简式是 .
.
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 g Fe与足量稀HNO3发生反应,转移的电子数为0.3 NA | |
| B. | 在1 L 0.1 mol/L AlCl3溶液中含有0.1 NA 个Al3+ | |
| C. | 在某密闭容器中盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应后,可得0.2NA个NH3分子 | |
| D. | 标准状况下,11.2 L四氯化碳中含有的C-Cl键的个数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com