
 �����£���10mL0.1mol?L-1NaOH��Һ����μ���0.1mol?L-1������Һ�����õζ�������ͼ��ʾ������˵����ȷ���ǣ�������
�����£���10mL0.1mol?L-1NaOH��Һ����μ���0.1mol?L-1������Һ�����õζ�������ͼ��ʾ������˵����ȷ���ǣ�������| A��pH=7ʱ�����Ӵ�����Һ�����Ϊ10mL |
| B��pH��7ʱ����Һ��c��CH3COO-����c��Na+�� |
| C��7��pH��13ʱ����Һ��c��Na+��+c��H+����c��CH3COOH��+c��OH-�� |
| D�������μ�0.1 mol?L-1������Һ����ҺpH���Ա�Ϊ1 |


 �ظ���ʦ�㲦ϵ�д�
�ظ���ʦ�㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ڢ� |
| C���٢ڢ� | D���ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�� |
| B���õ������ӵ����ֲ�ͬ����ͬʱ����Һ���У����γ�ԭ��� |
| C����ԭ����У�����������һ���Ǹ���������������Ӧ |
| D����ԭ��طŵ�ʱ���������Һ�е��������������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£���0.01mol?L-1NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�c��SO42-����c��Na+����c��NH4+����c��OH-��=c��H+�� |
| B����NaHY��ˮ��Һ�Լ��ԣ�����Һ������Ũ�ȹ�ϵΪ��c��Na+����c��OH-����c��H+����c��HY-�� |
| C��0.1 mol/L Na2CO3��Һ��c��OH-��=c��HCO3-��+c��H+��+2c��H2CO3�� |
| D�����ʵ�������0.1mol��HCN��NaCN��Ϻ����1L��Һ��c��HCN��+c��CN-��=0.1 mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ʵı�����һ��������� |
| B�����Ǻ���ѿ�ǵ�ˮ�������ȫ��ͬ |
| C������ؽ����Σ���������ţ�̻��ɽⶾ |
| D�����ࡢ֬�ࡢ�����ʶ�������Ȼ�߷��ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
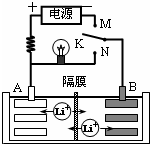 ��ͼ��һ�ֿɳ�������ӵ�س�ŵ�Ĺ���ʾ��ͼ���ŵ�ʱ�õ�صĵ缫��ӦʽΪ��������LixC6-xe-=C6+xLi+��LixC6��ʾ�ԭ��Ƕ��ʯī�γɵĸ��ϲ��ϣ�������Li1-xMnO2+xLi++xe-=LiMnO2��LiMnO2��ʾ���ԭ�ӵĶ������̣��������й�˵����ȷ���ǣ�������
��ͼ��һ�ֿɳ�������ӵ�س�ŵ�Ĺ���ʾ��ͼ���ŵ�ʱ�õ�صĵ缫��ӦʽΪ��������LixC6-xe-=C6+xLi+��LixC6��ʾ�ԭ��Ƕ��ʯī�γɵĸ��ϲ��ϣ�������Li1-xMnO2+xLi++xe-=LiMnO2��LiMnO2��ʾ���ԭ�ӵĶ������̣��������й�˵����ȷ���ǣ�������| A���������䡢�ŵ���������ٴ���3����ʽ������ת�� | |||
| B��K��M���ʱ��A��������������ԭ��Ӧ | |||
| C��K��N���ʱ��Li+��A����Ǩ�Ƶ�B���� | |||
D���õ�ص��ܷ�ӦʽΪLi1-xMnO2+LixC6
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����40 g NaOH����1 L ˮ���õ���Һ |
| B����0.5 mol?L-1��NaNO3��Һ100 mL ����������50 gˮ���õ���Һ |
| C����23 g NaCl ����ˮ�����1 L����Һ |
| D����K+Ϊ2 mol?L-1��K2SO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ϩ������ȩ��֬ |
| B����ѿ�ǡ� �ȵ��� |
| C������ �������ϩ |
| D����ά�ء� ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��S |
| B��H2S |
| C��SO2 |
| D��SO3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com