
【题目】已知:lg C(s)燃烧生成一氧化碳放出9.2kJ的热量;氧化亚铜与氧气反应的能量变化如图所示。下列叙述正确的是

A. 碳[C(s)]的燃烧热△H为 -110.4kJ·mol-1
B. 1mol CuO分解生成Cu2O放出73kJ的热量
C. 反应2Cu2O(s)+O2(g)=4CuO(s)的活化能为292 kJ·mol-1
D. 足量炭粉与CuO反应生成Cu2O的热化学方程式为:C(s)+2CuO(s)=Cu2O(s) +CO(g) △H= +35.6kJ·mol-1
【答案】D
【解析】
A碳[C(s)]的燃烧热指的是1mol碳完全燃烧生成二氧化碳气体时所放出的热量,根据题中数据无法计算碳的燃烧热,故A不正确;
B.由题图可知,氧化亚铜与氧气反应生成CuO是放热反应,则CuO分解生成Cu2O是吸热反应,故B错误;
C.由题图可知氧化亚铜与氧气反应生成CuO的活化能为348 kJ·mol-1,故C错误;
D.将lg C(s)燃烧生成一氧化碳放出9.2kJ的热量的热化学方程式为:①C(s)+1/2O2(g)=CO(g)△H= -110.4kJ·mol-1,氧化亚铜与氧气反应的热化学方程式为:②2Cu2O + O2(g)=4CuO(s)△H= -292kJ·mol-1,根据盖斯定律计算①-②/2得热化学方程式为C(s)+2CuO(s)=Cu2O(s) +CO(g) △H= +35.6kJ·mol-1,故正确。
故选D。


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】某同学在常温下设计以下实验流程探究Na2S2O3的化学性质。下列说法正确的是

A. 实验①说明Na2S2O3溶液中水电离的c(OH-)=10-8mol·L-1
B. Na2S2O3溶液pH=8的原因用离子方程式表示为S2O32-+2H2O![]() H2S2O3+2OH-
H2S2O3+2OH-
C. 生成的沉淀B可能是BaSO3或BaSO4,要进一步确认还需加入稀硝酸验证
D. 实验②说明Na2S2O3具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g) 达到平衡。下列说法正确的是
CH3OH(g) 达到平衡。下列说法正确的是

A. 该反应的正反应放热
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多硫化物是含多硫离子(Sx2-)的化合物,可用作废水处理剂、硫化剂等。回答下列问题:
(1)多硫化钠(Na2S5)可由H2S与Na2S在一定条件下反应制得,该反应的还原产物为___________,Na2S5中含有的化学键类型是______________________。
(2)多硫化物MS4溶液在碱性条件下可高效处理高浓度含CN-电镀废水,CN-被氧化成毒性较小的SCN-,S2-转化为S2-。
①M的离子与S2-具有相同的核外电子排布,则M在周期表中的位置是___________。
②CN-的电子式为______________________。
③处理废水的离子方程式为______________________。
(3)过硫化铵[(NH4)2S2]可用作硫化试剂,为探究其性质,某研究小组进行如下实验:取含1.00g(NH4)2S2的溶液加入足量稀硫酸酸化,得到0.32g淡黄色不溶物A和氢化物B。
①A是___________,生成的B在标准状况的体积为___________mL。
②利用(NN4)2S2溶液中的活性硫能将硫锡矿中的难溶物硫化亚锡(II)(SnS)氧化成硫代锡(IV)酸铵[(NH4)2SnS3]而溶解,写出反应的离子方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的由Cu和Cu2O组成的混合粉末加入到125 mL 2.6 mol·L-1的硝酸中,固体恰好完全溶解,得蓝色溶液X并收集到V mL(标准状况)的纯净无色气体Y。下列结论正确的是( )
A. X中有两种溶质
B. Y通入纯水中得到酸性溶液
C. 原混合粉末的总质量小于7.8 g
D. 当V=1 680时,原混合粉末中Cu和Cu2O的物质的量之比为8∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 常温下,反应C(s)+CO2(g) ![]() 2CO(g)不能自发进行,则该反应的ΔH>0
2CO(g)不能自发进行,则该反应的ΔH>0
B. 向醋酸中加水稀释,溶液中所有离子浓度均减小
C. 溶度积常数Ksp与温度有关,温度越高,溶度积越大
D. 吸热反应在常温下不能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。气态时,已知断裂1mol N—N键吸收193kJ热量,断裂1mol N≡N键吸收941kJ热量,则( )
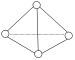
A. N4与N2互称为同位素 B. 1mol N4气体转化为N2时要吸收748kJ能量
C. N4是N2的同系物 D. 1mol N4气体转化为N2时要放出724kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com