
”¾ĢāÄæ”æŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅæÉÄÜ·¢Éś»Æѧ·“Ó¦£¬ÕāŠ©·Ö×Ó±»³ĘĪŖ»ī»Æ·Ö×Ó”£Ź¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ潊»ī»ÆÄÜ£¬Ę䵄Ī»Ķس£ÓĆkJmol£1±ķŹ¾”£ĒėČĻÕę¹Ū²ģĶ¼1£¬Č»ŗó»Ų“šĪŹĢā”£
£Ø1£©Ķ¼ÖŠĖłŹ¾·“Ó¦ŹĒ________£ØĢī”°ĪüČČ”±»ņ”°·ÅČČ”±£©·“Ó¦”£

£Ø2£©ŅŃÖŖ²šæŖ1mol H©H¼ü”¢1mol I©I”¢1mol H©I¼ü·Ö±šŠčŅŖĪüŹÕµÄÄÜĮæĪŖ436kJ”¢151kJ”¢299kJ”£ŌņÓÉ1molĒāĘųŗĶ1mol µā·“Ӧɜ³ÉHI»į________£ØĢī”°·Å³ö”±»ņ”°ĪüŹÕ”±£©________kJµÄČČĮ攣ŌŚ»Æѧ·“Ó¦¹ż³ĢÖŠ£¬ŹĒ½«________×Ŗ»ÆĪŖ________”£
£Ø3£©Ä³ŹµŃ銔×éĶ¬Ń§½ųŠŠČēĶ¼2µÄŹµŃ飬ŅŌĢ½¾æ»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»Æ”£ŹµŃé±ķĆ÷£ŗ¢ŁÖŠµÄĪĀ¶Č½µµĶ£¬ÓÉ“ĖÅŠ¶ĻĒāŃõ»Æ±µ¾§ĢåÓėĀČ»Æļ§¾§Ģå·“Ó¦ŹĒ________£ØĢī”°ĪüČČ”±»ņ”°·ÅČČ”±£©·“Ó¦£»ŹµŃé¢ŚÖŠ£¬øĆŠ”×éĶ¬Ń§ŌŚÉÕ±ÖŠ¼ÓČė5mL 1.0mol/LŃĪĖį£¬ŌŁ·ÅČėÓĆÉ°Ö½“ņÄ„¹żµÄĀĮĢõ£¬øĆ·“Ó¦ŹĒ________£ØĢī”°ĪüČČ”±»ņ”°·ÅČČ”±£©·“Ó¦”£
”¾“š°ø”æ·ÅČČ ·Å³ö 11 »ÆѧÄÜ ČČÄÜ ĪüČČ ·ÅČČ
”¾½āĪö”æ
(1)ŅĄ¾ŻĶ¼Ļó·ÖĪö·“Ó¦ĪļµÄÄÜĮæ“óÓŚÉś³ÉĪļµÄÄÜĮ棬·“Ó¦·ÅČČ£»
(2)ŌŚ·“Ó¦H2+I22HIÖŠ£¬¶ĻĮŃ1molH-H¼ü£¬1molI-I¼ü¹²ĪüŹÕµÄÄÜĮæĪŖ£ŗ1”Į436kJ+151kJ=587kJ£¬Éś³É2molHI£¬¹²ŠĪ³É2molH-I¼ü£¬·Å³öµÄÄÜĮæĪŖ£ŗ2”Į299kJ=598kJ£¬ĪüŹÕµÄÄÜĮæÉŁ£¬·Å³öµÄÄÜĮæ¶ą£¬ĖłŅŌøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬·Å³öµÄČČĮæĪŖ£ŗ598kJ-587kJ=11kJ£¬ŌŚ»Æѧ·“Ó¦¹ż³ĢÖŠ£¬½«»ÆѧÄÜ×Ŗ»ÆĪŖČČÄÜ£»
(3)¢ŁÖŠµÄĪĀ¶Č½µµĶĖµĆ÷øĆ·“Ó¦ŹĒĪüČČ·“Ó¦£»»īĘĆ½šŹōÖĆ»»ĖįÖŠĒāµÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNAŹĒ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. 11g³¬ÖŲĖ®(T2O)ŗ¬ÖŠ×ÓŹżĪŖ5NA
B. 25”ę£¬pH=13µÄ1L Ba(OH)2ČÜŅŗÖŠOH”ŖµÄŹżÄæĪŖ0.2NA
C. 1mol½šøÕŹÆÖŠC”ŖC¼üµÄŹżÄæĪŖ2NA
D. ³£ĪĀĻĀ£¬pH=6µÄMgCl2ČÜŅŗÖŠH+µÄŹżÄæĪŖ10-6NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚ°¢·ü¼ÓµĀĀŽ³£ŹżµÄĖµ·ØÖŠ²»ÕżČ·µÄŹĒ£Ø £©
A.6.02”Į1023½Š×ö°¢·ü¼ÓµĀĀŽ³£Źż
B.12g12Cŗ¬ÓŠµÄĢ¼Ō×ÓŹż¾ĶŹĒ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ
C.ŗ¬ÓŠ°¢·ü¼ÓµĀĀŽ³£ŹżÖµøöĪ¢Į£µÄĪļÖŹŹĒ1mol
D.1.5molH2Oŗ¬ÓŠ9.03”Į1023øöĖ®·Ö×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶Ō½šŹōÖĘĘ·½ųŠŠæ¹øÆŹ““¦Ąķ£¬æÉŃÓ³¤ĘäŹ¹ÓĆŹŁĆü”£ŅŌĻĀĪŖĀĮ²Ä±ķĆꓦĄķµÄŅ»ÖÖ·½·Ø£ŗ
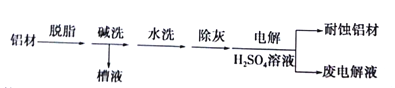
£Ø1£©¼īĻ“µÄÄæµÄŹĒ³żČ„ĀĮ²Ä±ķĆęµÄ×ŌČ»Ńõ»ÆĤ£¬¼īĻ“Ź±³£ÓŠĘųÅŻĆ°³ö£¬ŌŅņŹĒ______£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©”£ĪŖ½«¼īĻ“²ŪŅŗÖŠµÄĀĮŅŌ³ĮµķŠĪŹ½»ŲŹÕ£¬×īŗĆĻņ²ŪŅŗÖŠ¼ÓČėĻĀĮŠÖŠµÄ______”£
a.![]() b.
b.![]() c.
c.![]() d.
d.![]()
£Ø2£©ŅŌĀĮ²ÄĪŖŃō¼«£¬ŌŚ![]() ČÜŅŗÖŠµē½ā£¬ĀĮ²Ä±ķĆęŠĪ³ÉŃõ»ÆĤ£¬Ńō¼«µē¼«·“Ó¦Ź½ĪŖ______
ČÜŅŗÖŠµē½ā£¬ĀĮ²Ä±ķĆęŠĪ³ÉŃõ»ÆĤ£¬Ńō¼«µē¼«·“Ó¦Ź½ĪŖ______
ȔɣĮæ·Ļµē½āŅŗ£¬¼ÓČė![]() ČÜŅŗŗó²śÉśĘųÅŻŗĶ°×É«³Įµķ£¬²śÉś³ĮµķµÄŌŅņŹĒ______£ØÓĆ»ÆѧÓĆÓļ»Ų“š£©
ČÜŅŗŗó²śÉśĘųÅŻŗĶ°×É«³Įµķ£¬²śÉś³ĮµķµÄŌŅņŹĒ______£ØÓĆ»ÆѧÓĆÓļ»Ų“š£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĢ½¾æĀĮʬ£ØĪ““ņÄ„£©ÓėNa2CO3ČÜŅŗµÄ·“Ó¦£¬ŹµŃéČēĻĀ£ŗ
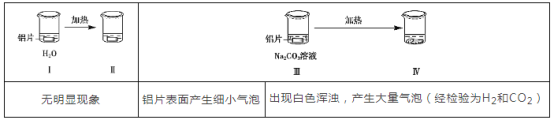
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A. Na2CO3ČÜŅŗÖŠ“ęŌŚĖ®½āĘ½ŗā£ŗCO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
B. ¶Ō±Č¢ń”¢¢ó£¬ĶĘ²āNa2CO3ČÜŅŗÄÜĘĘ»µĀĮ±ķĆęµÄŃõ»ÆĤ
C. ¢ōČÜŅŗÖŠæÉÄÜ“ęŌŚ“óĮæAl3+
D. ĶĘ²ā³öĻÖ°×É«»ė×ĒµÄæÉÄÜŌŅņ£ŗAlO2-+HCO3-+H2O=Al(OH)3”ż+CO32-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷·“Ó¦“ļµ½»ÆŃ§Ę½ŗā£¬¼ÓŃ¹»ņ½µĪĀ¶¼ÄÜŹ¹»ÆŃ§Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶ÆµÄŹĒ
A. 2NO2![]() N2O4£ØÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦£© B. C£Øs£©+CO2
N2O4£ØÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦£© B. C£Øs£©+CO2![]() 2CO£ØÕż·“Ó¦ĪŖĪüČČ·“Ó¦£©
2CO£ØÕż·“Ó¦ĪŖĪüČČ·“Ó¦£©
C. N2+3H2![]() 2NH3£ØÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦£© D. H2S
2NH3£ØÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦£© D. H2S![]() H2+S£Øs£©£ØÕż·“Ó¦ĪŖĪüČČ·“Ó¦£©
H2+S£Øs£©£ØÕż·“Ó¦ĪŖĪüČČ·“Ó¦£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø10·Ö£©ĀĮŌŖĖŲŌŚ×ŌČ»½ēÖŠÖ÷ŅŖ“ęŌŚÓŚĀĮĶĮæó£ØÖ÷ŅŖ³É·ÖĪŖAl2O3£¬»¹ŗ¬ÓŠFe2O3”¢FeO”¢SiO2£©ÖŠ”£¹¤ŅµÉĻÓĆĀĮĶĮæóÖʱøĀĮµÄijÖÖ»ÆŗĻĪļµÄ¹¤ŅÕĮ÷³ĢČēĻĀ”£

£Ø1£©ŌŚĀĖŅŗAÖŠ¼ÓČėĘÆ°×Ņŗ£¬ÄæµÄŹĒŃõ»Æ³żĢś£¬ĖłµĆĀĖŅŗBĻŌĖįŠŌ”£
¢Ł¼ģŃéĀĖŅŗBÖŠŹĒ·ń»¹ŗ¬ÓŠĢśŌŖĖŲµÄ·½·ØĪŖ£ŗ £Ø×¢Ć÷ŹŌ¼Į”¢ĻÖĻ󣩔£
¢Ś½«ĀĖŅŗBÖŠµÄĀĮŌŖĖŲŅŌ³ĮµķŠĪŹ½Īö³ö£¬æÉŃ”ÓƵÄ×īŗĆŹŌ¼ĮĪŖ £ØĢī“śŗÅ£©”£
a£®ĒāŃõ»ÆÄĘČÜŅŗ b£®ĮņĖįČÜŅŗ c£®°±Ė® d£®¶žŃõ»ÆĢ¼
¢ŪÓÉĀĖŅŗBÖʱøĀČ»ÆĀĮ¾§ĢåÉę¼°µÄ²Ł×÷ĪŖ£ŗ±ßµĪ¼ÓÅØŃĪĖį±ßÕō·¢ÅØĖõ”¢ĄäČ“½į¾§”¢
£ØĢī²Ł×÷Ćū³Ę£©”¢Ļ“µÓ”£
¢ÜøĆ¹ż³ĢÖŠÉę¼°Ä³Ńõ»Æ»¹Ō·“Ó¦ČēĻĀ£¬ĒėĶź³ÉÅäĘ½£ŗ
Fe2++ ClO£+ = Fe(OH)3”ż+ C1£+
£Ø2£©SiO2ŗĶNaOH±ŗÉÕÖʱø¹čĖįÄĘ£¬æɲÉÓƵÄ×°ÖĆĪŖ £ØĢī“śŗÅ£©”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆ·Ļ¾É¶ĘŠæĢśĘ¤æÉÖʱø“ÅŠŌFe3O4½ŗĢåĮ£×Ó¼°ø±²śĪļZnO,ÖʱøĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ

(1)“ÓĮ÷³ĢĶ¼æÉÖŖ,Zn”¢FeÖŠÄÜÓėNaOHČÜŅŗ·“Ó¦µÄŹĒ________”£
(2)Zn(OH)2³Įµķ¼ÓČČæɵĆZnO,øĆ·“Ó¦______£ØĢī”°ŹĒ”±»ņ”°²»ŹĒ”±£©Ńõ»Æ»¹Ō·“Ó¦”£
(3)Ļņ²»ČÜĪļÖŠ¼ÓČėĻ”H2SO4·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ_________”£
(4)¼ÓČėŹŹĮæH2O2µÄÄæµÄŹĒ_________”£
(5)ČēŗĪÖ¤Ć÷ŅŃÉś³ÉĮĖFe3O4½ŗĢå? _________”£
(6)Į÷³ĢÖŠĖłŠčµÄĮņĖįČÜŅŗÓɽ¹ĮņĖį(H2SO4”¤SO3)ČÜÓŚĖ®ÅäÖʶų³É£¬ĘäÖŠµÄSO3¶¼×Ŗ»ÆĪŖĮņĖį£¬Čō½«445g½¹ĮņĖįČÜÓŚĖ®Åä³É4.00L ĮņĖį£¬øĆĮņĖįµÄĪļÖŹµÄĮæÅضČĪŖ______mol/L”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±źŗÅĪŖ¢Ł”«¢āµÄŌŖĖŲ£¬ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĻĀ£ŗ
Ö÷×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0×å |
1 | ¢Ł | ¢Ś | ||||||
2 | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ||||
3 | ¢ß | ¢ą | ¢į | ¢ā |
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öŌŖĖŲ¢ŪµÄĆū³Ę__”£
£Ø2£©¢ŁŗĶ¢ÜŗÅŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ__£¬ÓƵē×ÓŹ½±ķŹ¾ĘäŠĪ³É¹ż³ĢĪŖ__”£
£Ø3£©¢ßŗĶ¢ąŗÅŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌŹĒ£ŗ__©__
£Ø4£©¢Ł”¢¢Ż”¢¢ßŗÅŌŖĖŲŠĪ³ÉµÄŅ»ÖÖ»ÆŗĻĪļµÄµē×ÓŹ½ŹĒ__£¬ŌŚøĆ»ÆŗĻĪļÖŠ¼Čŗ¬ÓŠ__¼ü£¬ÓÖŗ¬ÓŠ__¼ü”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com