
下列叙述中错误的是( )
A.海洋是一个巨大的资源宝库
B.海水中含量最多的盐是NaCl
C.地球上99%以上的溴元素以单质形式存在于海洋中
D.海水是镁元素的一个重要来源
科目:高中化学 来源: 题型:
理论上不能设计原电池的化学反应是( )
A.CH4+2O2―→CO2+2H2O
B.HNO3+NaOH===NaNO3+H2O
C.2H2+O2===2H2O
D.2FeCl3+Fe===3FeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
你认为减少酸雨产生的途径可采用的措施是( )
①少用煤作燃料 ②把工厂烟卤造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤
C.①③⑤ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的性质和用途错误的是( )
A.氧化铁是一种红棕色粉末,常用于制油漆和涂料
B.氧化铝是一种耐火材料,常用于制造耐火坩埚和耐火砖
C.氧化铜呈红色,可作为制造陶瓷的红色颜料
D.明矾可作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
由海水制取无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A.①③⑤③① B.③②④①⑤
C.③④②⑤① D.②④③⑤①
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下进行下列实验:甲、乙、丙各取30 mL同浓度的盐酸,加入不同质量的同一镁铝合金粉末,有关数据列表如下:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 765 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
(1)盐酸的物质的量浓度是多少?
(2)求合金中镁、铝的质量分数。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
把煤作为燃料可通过下列两种途径。
途径Ⅰ:C(s)+O2(g)====CO2(g) ΔH=-Q1 kJ·mol-1
途径 Ⅱ:先制水煤气: C(s)+H2O(g)====CO(g)+H2(g) ΔH=+Q2 kJ·mol-1
再燃烧水煤气:2CO(g)+O2(g)====2CO2(g);2H2(g)+O2(g)====2H2O(g)
ΔH=-Q3 kJ·mol-1
试回答下列问题:
(1)途径Ⅰ放出的热量________(填“>”“=”或“<”)途径Ⅱ放出的热量。
(2)Q1、Q2、Q3的数学关系式是_____ __________。
__________。
(3)由于制取水煤气的反应里,反应物所具有的总能量____________(填“>”“=”或“<”)产物所具有的总能量,因此在化学反应里,反应物就需要_______能量才能转化为产物,因此其反应条件为_________ __________________________。
__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某强酸性溶液X可能含有Ba2+、Al3+、NH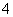 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO 、SO
、SO 、SO
、SO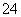 、Cl-、NO
、Cl-、NO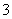 中的一种或几种,取该溶液进行连续实验,实验过程如下:
中的一种或几种,取该溶液进行连续实验,实验过程如下:
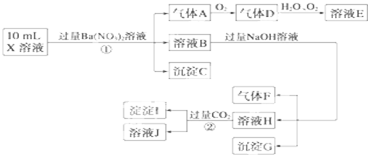
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是___▲___,不能确定是否含有的离子(M)是___▲___,若要确定该M(若不止一种,可任选一种)在溶液X中不存在,最可靠的化学方法是__▲____.
(2)写出反应②的离子方程式:___▲___.
(3)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式___▲___.
(4)假设测定A、F、I均为0.1mol,10mL X溶液中n(H+)=0.4mol,当沉淀C物质的量大于0.7mol时,溶液X中还一定含有___▲___.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com