
常温下向1L 0.1mol·L-1NH4C1溶液中,不断加入NaOH固体后,NH4+与NH3·H2O浓度的变化趋势如右图所示(不考虑溶液体积变化和氨气的挥发),下列说法不正确的是
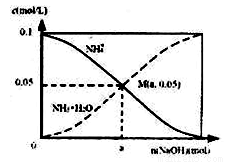
A.M点溶液中水的电离程度比原溶液小
B.在M点时,n(OH-)-n(H+)=(a-0.05)mol
C.随着NaOH的加入,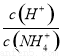 不断减小
不断减小
D.当n(NaOH)=0.1mol时, c(OH-)>c(Cl-)>c(NH3·H2O)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年湖北市高一5月月考化学试卷(解析版) 题型:选择题
一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g) Y(g)+Z(g),达到反应限度的标志是
Y(g)+Z(g),达到反应限度的标志是
①X的分解速率与X的生成速率相等 ②反应容器中压强不再变化
③X、Y、Z的浓度不再变化 ④单位时间内生成1molY的同时生成1molZ
A.①③ B.②③ C.①② D.②④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学孔德校区高二下6月考化学卷(解析版) 题型:实验题
化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。下列装置是用燃烧法确定有机物分子式常用的装置。

(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是 。
(2)C装置中浓硫酸的作用是 。
(3)D装置中MnO2的作用是 。
(4)燃烧管中CuO的作用是 。
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92 g样品,经充分反应后,A管质量增加1.76 g,B管质量增加1.08 g,则该样品的实验式为 。
(6)用质谱仪测定其相对分子质量,得如图一所示的质谱图,则该有机物的相对分子质量为 。
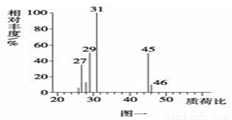
(7)能否根据A的实验式确定A的分子式 (填“能”或“不能”),若能,则A的分子式是 (若不能,则此空不填)。
(8)该物质的核磁共振氢谱如图二所示,则其结构简式为 。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学孔德校区高二下6月考化学卷(解析版) 题型:选择题
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三5月高考拉练一模理综化学试卷(解析版) 题型:实验题
工业上可由A和环己烯( )为原料合成某重要的有机物X、Y,路线如下(部分反应条件略):
)为原料合成某重要的有机物X、Y,路线如下(部分反应条件略):

(1)B中含氧官能团的名称是___________。
(2)A的结构简式是______________。
(3)任选1种具有反式结构的C的同系物,用结构简式表示其反式结构_______。
(4)反应②、③、④、⑤中与反应①的类型相同的是_________。
(5)G→H的化学方程式是__________。
(6)E的结构简式是________________。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三5月高考拉练一模理综化学试卷(解析版) 题型:选择题
下列化学用语表示正确的是
A.中子数为20的氯原子:
B.二氧化硅的分子式:SiO2
C.硫化氢的结构式:H—S—H
D.氯化铵的电子式:
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川二中高三5月适应性训练理综化学试卷(解析版) 题型:填空题
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g)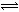 2SO3(g) ΔH=-196.6 kJ·mol—1,2NO(g)+O2(g)
2SO3(g) ΔH=-196.6 kJ·mol—1,2NO(g)+O2(g)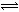 2NO2(g) ΔH=-113.0 kJ·mol—1,则反应:NO2(g)+SO2(g)
2NO2(g) ΔH=-113.0 kJ·mol—1,则反应:NO2(g)+SO2(g)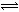 SO3(g)+NO(g)的ΔH= kJ·mol—1
SO3(g)+NO(g)的ΔH= kJ·mol—1
(2)利用反应6NO2+ 8NH3 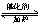 7N2+12H2O可处理NO2。一定条件下,将该反应设计成如右图所示装置,其中电极均为石墨,使用熔融金属氧化物作电解质,写出负极电极反应式 ;若一段时间内测得外电路中有1.2mol电子通过,则两极共产生的气体产物在标准状况下的体积为 L。
7N2+12H2O可处理NO2。一定条件下,将该反应设计成如右图所示装置,其中电极均为石墨,使用熔融金属氧化物作电解质,写出负极电极反应式 ;若一段时间内测得外电路中有1.2mol电子通过,则两极共产生的气体产物在标准状况下的体积为 L。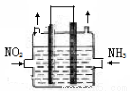
(3)一定条件下,将NO2与SO2以体积比1︰2置于恒容密闭容器中发生下述反应:NO2(g)+SO2(g)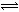 SO3(g)+NO(g),下列能说明该反应达到平衡状态的是 。
SO3(g)+NO(g),下列能说明该反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的物质的量比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
(4)CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)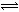 CH3OH(g)。一定温度下,向容积为2L的密闭容器中充入2molCO和2molH2发生上述
CH3OH(g)。一定温度下,向容积为2L的密闭容器中充入2molCO和2molH2发生上述 反应,5min后反应平衡,此时测得CH3OH的浓度为0.3mol/L,计算反应开始至平衡时的平均速率v(H2)= ;该温度下反应的平衡常数为 (保留两位小数)。
反应,5min后反应平衡,此时测得CH3OH的浓度为0.3mol/L,计算反应开始至平衡时的平均速率v(H2)= ;该温度下反应的平衡常数为 (保留两位小数)。
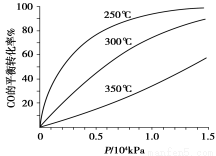
(5)不同温度CO的平衡转化率与压强的关系如上图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末化学试卷(解析版) 题型:选择题
取一只大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,用铁架台固定好。放在光亮处一段时间,下列对观察到的现象的描述及说明正确的是( )
A.试管中气体颜色变浅,是因为发生了加成反应
B.试管中有少量白雾生成,这是氯化氢的小液滴
C.试管内壁出现油状液体,这是甲烷与氯气的混合溶液
D.试管内壁出现油状液体,这是CH3Cl小液滴
查看答案和解析>>
科目:高中化学 来源:2016届湖北省沙市高三高考前最后一卷理综化学试卷(解析版) 题型:填空题
碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式_________________。
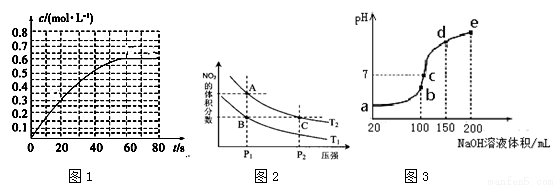
(2)298 K时,在2L恒容密闭容器中发生反应:2NO2(g) N2O4(g)ΔH=-a kJ·mol-1 (a>0)。N2O4的物质的量浓度随时间变化如图1。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题。
N2O4(g)ΔH=-a kJ·mol-1 (a>0)。N2O4的物质的量浓度随时间变化如图1。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题。
①298k时,该反应的平衡常数为________。
②在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示。
下列说法正确的是( )
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol 、n(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图3所示。试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是__________(填“a”“b”“c”“d”或“e”,下同)
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com