
含A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)在元素周期表中,A位于________族,与A同族但相对原子质量比A小的元素B的原子结构示意图为__________________,A与B在原子的电子层结构上的相同点是________________________________________________________________________
________________________________________________________________________。
(2)易与C发生化学反应的酸是________(写名称),反应的化学方程式是________________________________________________________________________。
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①写出生成D和F的化学反应方程式:___________________________________。
②要将纯碱高温熔化,下列坩埚中可选用的是________。
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
(4)100 g C与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是____________________。
答案 (1)ⅣA  最外层均有4个电子,最内层均有2个电子
最外层均有4个电子,最内层均有2个电子
(2)氢氟酸 SiO2+4HF===SiF4↑+2H2O
(3)①SiO2+Na2CO3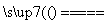 Na2SiO3+CO2↑,Na2SiO3+CO2+H2O===Na2CO3+H2SiO3↓ ②D
Na2SiO3+CO2↑,Na2SiO3+CO2+H2O===Na2CO3+H2SiO3↓ ②D
(4)50%
解析 (1)A元素单质可作半导体材料,含A元素的某化合物是制造光导纤维的原料,可知A为硅元素,C为SiO2,D为Na2SiO3。比硅相对原子质量小的同族元素B为碳。(2)C为SiO2,能与SiO2反应的酸只有氢氟酸。(3)SiO2与Na2CO3高温下反应生成Na2SiO3和CO2,含SiO2的材料(普通玻璃、石英玻璃)以及Al2O3等都能与Na2CO3在高温下反应,故不能用以上材质的坩埚熔融Na2CO3。(4)若SiO2恰好完全反应或过量,与CaCO3反应的化学方程式只有一个,即CaCO3+SiO2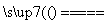 CaSiO3+CO2↑。若CaCO3过量,除发生上述反应外,还会发生反应:CaCO3
CaSiO3+CO2↑。若CaCO3过量,除发生上述反应外,还会发生反应:CaCO3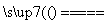 CaO+CO2↑。总之,CaCO3的多少决定了CO2的产量,可通过以下关系列式求解:
CaO+CO2↑。总之,CaCO3的多少决定了CO2的产量,可通过以下关系列式求解:
CaCO3 ~ CO2
100 g 22.4 L
m(CaCO3) 11.2 L
m(CaCO3)=50 g
混合物中CaCO3的质量分数: ×100%=50%。
×100%=50%。


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500 ℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
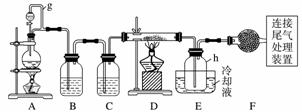
相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式:________________________________________________________________________。
(2)装置A中g管的作用是____________;装置C中的试剂是__________;装置E中的h瓶需要冷却的理由是_______________________________。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是______________________(填写元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后得到的固体物质是( )
A.Na2SiO3 B.Na2CO3、Na2SiO3
C.Na2CO3、SiO2 D.SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式为 ( )。
A.碳酸氢钠溶液中滴入氢氧化钙溶液:HCO +OH-===CO
+OH-===CO +H2O
+H2O
B.二氧化硫通入次氯酸钠溶液:SO2+ClO-+OH-===SO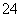 +Cl-+H2O
+Cl-+H2O
C.硫化钡加入稀硫酸:BaS+2H+===H2S↑+Ba2+
D.新制的氧化铝可溶于氢氧化钠溶液:Al2O3+2OH-+H2O===
2[Al(OH)4]-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:NH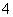 、Ba2+、Na+、H+、SO
、Ba2+、Na+、H+、SO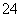 、NO
、NO 、OH-、CO
、OH-、CO 。将这四种溶液分别标记为A、B、C、D,进行如下实验:
。将这四种溶液分别标记为A、B、C、D,进行如下实验:
①在A或D中滴入C,均有沉淀生成;
②D和B反应生成的气体能被A吸收;
③A和D反应生成的气体能被B吸收。
试回答下列问题:
(1)D的化学式是______,判断理由是__________________________________________________
__________________________________________________。
(2)写出其余几种物质的化学式:A____________________,B____________________,C____________________。
(3)写出实验②中有关反应的离子方程式__________________________________________________
__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
饱和氯水与石灰石的反应是制取较浓的HClO溶液的方法之一。某同学运用这一方法,尝试制取HClO溶液并进行了如下定性实验:
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水,充分反应,有少量气泡产生,溶液的黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立刻产生大量气泡;
第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2气体。
(1)试解释可以在饱和氯水中加入石灰石制备HClO的原因:________________________________________________________________________
________________________________________________________________________。
(2)写出步骤③中第一份及第二份滤液发生反应的离子方程式:
第一份________________________________________________________________________;
第二份________________________________________________________________________。
(3)试根据所学知识推测,在②的滤液中含有的溶质,除了溶解的极少量氯气外,还含有的其他溶质为(写化学式)__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对充有氖气的霓虹灯管通电,灯管发出红色光。产生这一现象的主要原因是( )
A.电子由激发态向基态跃迁时以光的形式释放能量
B.电子由基态向激发态跃迁时吸收除红光以外的光线
C.氖原子获得电子后转变成发出红光的物质
D.在电流的作用下,氖原子与构成灯管的物质发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com