
【题目】下列有关氯水的叙述,正确的是( )
A.新制氯水中只含有氯气和次氯酸分子
B.新制氯水可使紫色石蕊试液先变红后褪色
C.氯水光照时有气泡逸出,该气体的主要成分是氯气
D.氯水放置数天后,其导电能力减弱
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+B(g)![]() 2C(g)+2D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是
2C(g)+2D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是
A. V(A)=0.4mol/(L·min) B. V(B)=0.5mol/(L·min)
C. V(C)=0.5mol/(L·min) D. V(D)=0.02mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列溶液的微粒浓度关系正确的是
A. pH = 5的H2C2O4溶液中: c(H+) = c(HC2O4-) = 1×10-5mol·L-1
B. 氨水稀释10倍后,其c(OH-)大于原来的![]()
C. pH之和为14的 H2S与NaOH 溶液混合:c(Na+)+c(H+) = c(OH-)+c(HS-)
D. (NH4)2SO4溶液和NaOH溶液混合所得的中性溶液中:c(Na+)< c(NH3 H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸是植物(特别是草本植物)常具有的成分,具有广泛的用途。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
I.拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为________(填字母序号)。
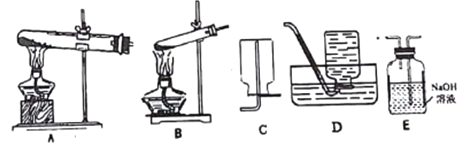
Ⅱ.设计实验证明草酸为弱酸的方案及其现象均正确的有______(填序号)。
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH>7;
C. 室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL
Ⅲ.医学上常用酸性KMnO4溶液和草酸(H2C2O4)溶液反应来测血液中血钙的含量。测定方法是:取2mL血液用蒸馏水稀释后.向其中加入足量的(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①溶解沉淀时______(填“能”或“不能”)用稀盐酸,原因是_________。
②滴定时,用______(填“酸”或“碱”)式滴定管装KMnO4溶液,滴定达到终点的现象是______。
③ 滴定过程中发生的离子反应方程式______________。
④ 若上述滴定中消耗了1.0×10-4mol/LKMnO4的溶液20mL,则200mL该血液中含钙_____g。
⑤ 下列操作会引起测定结果偏高的是__________(填序号)
A.滴定管在盛装KMnO4溶液前未润洗
B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,没用待测液冲洗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界为人类提供了多种多样的营养物质,下列有关营养物质的说法正确的是
A. 蔗糖、淀粉、油脂等都可以发生水解反应
B. 摄入人体的纤维素在酶的作用下能水解为葡萄糖
C. 糖类、蛋白质、油脂都属于天然高分子化合物
D. 所有糖类物质都有甜味,但不一定都溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】印刷电路板在科技领域具有不可替代的作用,它的制备方法为高分子化合物和铜箔压合,通过FeCl3溶液“腐蚀”而成。某实验小组在实验室用废弃的印刷电路板和“腐蚀液”提取铜的一种工艺流程如下:
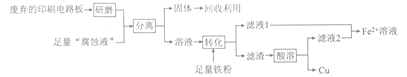
请回答下列问题:
(1) 检验“腐蚀液”中含有Fe2+的方法为_________________。
(2)“分离”所用的操作名称为____________,该操作所用的主要玻璃仪器有烧杯、_____________。
(3)用电解法在铁上镀铜时,阴极材料为_____________(填化学式),理论上电镀过程中电解质溶液的浓度_______________ (填“增大”“减小”或“不变”)。
(4) Fe2+溶液有很多重要用途。
①已知:常温下,Ksp[Fe(OH)2]=1.8×10-16。保存1.8mol·L-1的FeSO4溶液时,为确保溶液中不出现浑浊,应调节溶液的pH不超过_________________。
②Fe2+可使Ag+与Fe3+之间相互转化。一定温度下,0.1 mol·L-1的Fe(NO3)2溶液中,c(Fe3+)与c(Ag+)的关系如图所示:
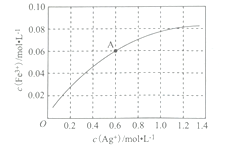
该温度下,A点溶液中转化反应的平衡常数为____________(溶液体积变化忽略不计);若将0.6mol·L-1 Fe(NO3)2溶液、0.15 mol·L-1 Fe(NO3)3溶液、0.06 mol L-1 AgNO3溶液等体积混合后,再加入1.08 g Ag,可观察到的现象为_________________________。
③Fe2+转化为Fe3+后,可用于制备高铁酸盐。向FeCl3溶液中加入NaOH、NaClO溶液制备Na2FeO4的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 液态HCl不导电,所以HCl是非电解质
B. NH3的水溶液能导电,所以NH3是电解质
C. 铜、石墨均能导电,所以它们都是电解质
D. 蔗糖在水溶液中和熔融时都不导电,所以是非电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com