
【题目】下列五种物质中,属于同系物的是
【答案】O2和O3;11H和21H;CH3CH2OH和CH3OCH3;CH4和 ![]() ;
;![]() 和CH3CH2CH2CH2CH3 .
和CH3CH2CH2CH2CH3 .
【解析】解:同系物:结构相似,在分子组成上相差一个或若干个CH2原子团的化合物,
A.O2和O3互为同素异形体,故错误;
B.11H和21H互为同位素,故错误;
C.CH3CH2OH和CH3OCH3互为同分异构体,故错误;
D.CH4和 ![]() 互为同系物,故正确;
互为同系物,故正确;
E. ![]() 和CH3CH2CH2CH2CH3互为同分异构体,故错误;
和CH3CH2CH2CH2CH3互为同分异构体,故错误;
故选D.
【考点精析】掌握芳香烃、烃基和同系物是解答本题的根本,需要知道分子里含有一个或多个苯环的碳氢化合物,称为芳香烃,其中由一个苯环和饱和烃基组成的芳香烃叫苯的同系物,其通式为CnH2n–6(n≥6).


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】按要求填空
(1)分析有机物的结构,有助于对其性质的掌握.
①有机物(CH3)3CCH2OH的名称为(填字母)
a.2,2﹣二甲基﹣1﹣丙醇 b.2,2,2﹣三甲基﹣2﹣乙醇 c.2,2﹣二甲基﹣2﹣丁醇
②下列化合物中不能使酸性高锰酸钾溶液褪色的是(填字母)
a、 ![]() ;b.CH≡CCH3; c、
;b.CH≡CCH3; c、 ![]()
③欲区分 ![]() 和
和 ![]() ,可选用(填字母)
,可选用(填字母)
a.AgNO3溶液 b.溴水 c.FeCl3溶液
(2)丹参素分子能抑制血小板的聚集,其结构简式为 ![]()
①丹参素分子中共平面的碳原子最少是个.
②1mol丹参素在一定条件下最多能与mol H2发生加成反应.
③丹参素的一种同分异构体(  )与足量溴水反应所得产物的结构简式为
)与足量溴水反应所得产物的结构简式为
(3)下面是某有机物中间体的部分合成路线: 
①A中含氧官能团的名称为和 .
②A与NaOH溶液在加热条件下发生反应后,有机产物的结构简式为
③B→C反应的类型为;该反应还可能产生另一种芳香族化合物(副产物),其结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、用0.1 molL-1 NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 molL-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

①滴定盐酸的曲线是______________(填“I”或“Ⅱ”);
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是_____________________;
③V1和V2的关系:V1 _____ V2(填“>”、“=”或“<”)。
Ⅱ、已知25℃时,2.0×103 mol/L氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F)与溶液pH的变化关系如图所示。

(1)25℃时,HF的电离平衡常数Ka=_____________。
(2)已知HF(aq)![]() H+(aq)+F(aq) ΔH=10.4 kJ/mol,现将室温下0.1 mol/L HF溶液升温至30℃(不考虑溶质和溶剂的挥发),下列各量增大的是__________。
H+(aq)+F(aq) ΔH=10.4 kJ/mol,现将室温下0.1 mol/L HF溶液升温至30℃(不考虑溶质和溶剂的挥发),下列各量增大的是__________。
a.Ka b.Kw c.n(H+) d. 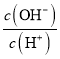
(3)25℃时,在20 mL 0.1 mol/L氢氟酸中加入V mL 0.1 mol/L NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是__________________。

a.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
b.①点时pH=6,此时溶液中,c(F)c(Na+)=9.9×107 mol/L
c.②点时,溶液中的c(F)=c(Na+)
d.③点时V=20 mL,此时溶液中c(F)<c(Na+)=0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学将金属钠露置于空气中,观察到下列现象:银白色→变灰暗→变白色→出现液滴→白色固体。其变质过程中不可能产生的物质是
A. Na2O B. NaOH
C. Na2CO3 D. NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于营养物质的说法正确的是( )
A. 油脂的氢化属于还原反应,又属于加成反应,生成物为纯净物
B. 1 mol蔗糖的水解产物是1 mol葡萄糖和1 mol果糖
C. 淀粉溶液和稀硫酸共热后发生水解反应,冷却后加少量银氨溶液,水浴加热后出现光亮的银镜
D. 鸡蛋白溶液中滴加饱和的硫酸铵溶液,出现白色沉淀,该过程叫做蛋白质的变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行试验并得到下表实验结果: 
序号 | A | B | 烧杯中的液体 | 灵敏电流计指针是否偏转 |
1 | Zn | Cu | 稀硫酸 | 有 |
2 | Zn | Cu | 乙醇 | 无 |
3 | Cu | C | 氯化钠溶液 | 有 |
4 | Mg | Al | 氢氧化钠溶液 | 有 |
分析上述数据,回答下列问题:
(1)实验1中电流由极流向极(填“A”或“B”)
(2)实验4中电子由B极 流向A极,表明负极是电极(填“镁”或“铝”)
(3)实验3 表明
A.铜在潮湿空气中不会被腐蚀
B.铜的腐蚀是会发生的
(4)分析上表有关信息,下列说法不正确的是
A.相对活泼的金属一旦做负极
B.失去电子的电极是负极
C.烧杯中的溶液,必须是电解质溶液
D.浸入同一电解质溶液中的两个电极,是活泼性不同的两种金属(或其中一种非金属)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂对工业污泥中的Cr元素回收与再利用的工艺如下(己知硫酸浸取液中的金属离子主要是Cr3+,其次是少量的Fe2+、Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3* | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时 的pH | 1.9 | 7.0 | — | 一 | — |
沉淀完全时 的pH | 3.2 | 9.0 | 11.1 | 8 | 9 (>9溶解) |
(1)实验室用98% (密度为1.84 g·cm-3)的浓硫酸配制200mL4.8 mol·L-1的硫酸溶液,配制时需要量取98%的浓硫酸的体积为_________mL (保留小数点后一位小数),所用的玻璃仪器除烧杯、玻璃棒、量筒外,还需__________________________________。
(2)在上述配制稀硫酸过程中,会导致所配溶液浓度偏小的操作是____________________(填序号)
a.定容时俯视刻度线 b.量取浓硫酸时,俯视刻度线
c.当容置瓶中液体占容积2/3左右时,未振荡摇匀 d.转移溶液时,没有等溶液冷却至室温
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr (CrO42-或Cr2O72-),以便于与杂质离子分离;另一方面是_____________________________。(离子方程式表示)
(4)调节溶液的pH=8除去的杂质离子是___________________。
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn +nNa+,被交换的杂质离子是_____________________。
(6)通SO2气体时,还原过程发生以下反应(填写缺项物质并配平)
____________________________________________________________Na2SO4.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化铝(AlON)是一种空间网状结构,硬度大熔点高的透明材料,描述正确的是
A.含有离子键B.属于原子晶体
C.既有离子键又有共价键D.属于离子晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com