
反应A(s)+2B(g)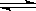 2C(g)在一密闭容器中进行,当改变下列条件之一时,一定能增大反应速率的是
2C(g)在一密闭容器中进行,当改变下列条件之一时,一定能增大反应速率的是
A.增加A物质的质量 B.降低温度
C.压缩反应容器体积 D.消耗掉部分B物质
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源:2014-2015学年河南省高三12月月考理综化学试卷(解析版) 题型:填空题
(14分)碳、氮及其化合物在工农业生产生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) =4NO(g)+CO2(g) + 2H2O(g) ΔH1=-574 kJ·molˉ1
CH4(g) + 4NO(g) = 2N2(g)+CO2(g) + 2H2O(g) ΔH2
若2 mol CH4 还原NO2 至N2,整个过程中放出的热量为1734 kJ,则ΔH2= ;
(2)据报道,科学家在一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应为:Fe2O3(s) + 3CH4(g) 2Fe(s) + 3CO(g) +6H2(g) ⊿H>0
2Fe(s) + 3CO(g) +6H2(g) ⊿H>0
①若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g。则该段时间内CO的平均反应速率为________________。
②若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是__________
A.CH4的转化率等于CO的产率
B.混合气体的平均相对分子质量不变
C.v(CO)与v(H2)的比值不变
D.固体的总质量不变
③该反应达到平衡时某物理量随温度变化如图所示,当温度由T1升高到T2时,平衡常数KA KB(填“>”、“<”或“=”)。纵坐标可以表示的物理量有哪些 。

A.H2的逆反应速率
B.CH4的的体积分数
C.混合气体的平均相对分子质量
D.CO的体积分数
(3)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:N2+3H2 2NH3,该过程中还原反应的方程式为 。
2NH3,该过程中还原反应的方程式为 。
(4)若往20mL 0.0lmol·L-l的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是

①该烧碱溶液的浓度为0.02mol·L-1
②该烧碱溶液的浓度为0.01mol·L-1
③HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO )>c(OH
)>c(OH )> c(H+)
)> c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
取四份碘水于试管中,编号为Ⅰ、Ⅱ、Ⅲ、Ⅳ,分别加入汽油、CCl4、酒精、NaCl溶液,振荡后静置,现象正确的是
A.Ⅰ中溶液分层,下层呈紫红色
B.Ⅱ中溶液分层,下层呈紫红色
C.Ⅲ中溶液分层,下层呈棕黄色
D.Ⅳ中溶液不分层,溶液呈无色
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
温度(℃) | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①写出工业合成氨的化学方程式 。
②由上表数据可知该反应为放热反应,理由是 。
③理论上,为了增大平衡时H2的转化率,可采取的措施是 。(填序号)
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2可通过反应 CH4(g) + H2O (g) CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的 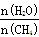 恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如下图所示:
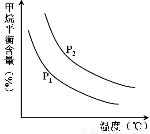
①图中,两条曲线表示压强的关系是:P1 P2(填“>”、“=”或“<”)。
②该反应为 反应(填“吸热”或“放热”)。
(3)原料气H2还可通过反应CO(g) + H2O(g)  CO2 (g) + H2(g) 获取。
CO2 (g) + H2(g) 获取。
①T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为 ,该反应平衡常数的表达式为 。
②保持温度仍为T ℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是 (填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n (CO) : n (H2O) : n (CO2) : n (H2) = 1 : 1 : 1 : 1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:选择题
25 ℃、101 kPa下:①2Na(s)+1/2O2(g)===Na2O(s) ΔH1=-414 kJ/mol
②2Na(s)+O2(g)===Na2O2(s) ΔH2=-511 kJ/mol
下列说法不正确的是
A.①和②产物的阴阳离子个数比相等 ,均为1:2
B.①和②生成等物质的量的产物,转移电子数相同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25 ℃、101 kPa下,Na2O2(s)+2Na(s)===2Na2O(s) ΔH=-317 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:选择题
对某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色无味的气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
C.加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH
D.向某溶液中加入AgNO3溶液,产生白色沉淀,则原溶液中有Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列说法错误的是
A.化学键的断裂和形成是化学反应中能量变化的主要原因
B.放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小
C.已知:S(s)+O2(g) = SO2(g) △H1 ;S(g)+O2(g) = SO2(g) △H2 ;则△H1>△H2
D.凡经加热而发生的化学反应都是吸热反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高一12月月考理综化学试卷(解析版) 题型:选择题
下列说法均摘自某些科普杂志,你认为无科学性错误的是
A.铅笔芯的原料是重金属铅,儿童在使用时不可以用嘴吮吸铅笔,以免引起铅中毒
B.CO有毒,生有煤炉的居室放置数盆清水,这样可有效的吸收CO,防止煤气中毒
C.汽水浇灌农田有一定的道理,其中二氧化碳的缓释,有利于作物的光合作用
D.纯碱又名烧碱,成分是氢氧化钠
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
由乙烯推测丙烯(CH3CH=CH2)的结构或性质正确的是
A.分子中3个碳原子在同一直线上 B.分子中所有原子在同一平面上
C.与氯化氢加成只生成一种产物 D.能发生加聚反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com