
| A. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O=2Cu↓+O2↑+4H+ | |
| B. | 惰性电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑ | |
| C. | 乙醛溶液中加入新制碱性Cu(OH)2悬浊液并加热CH3CHO+2 Cu(OH)2+OH-$\stackrel{△}{→}$ CH3COO-+Cu2O↓+3H2O | |
| D. | 硝酸银溶液中滴加过量氨水:Ag++NH3•H2O═AgOH↓+NH4+ |
分析 A.铜为活性电极,电极本身放电;
B.惰性电极电解MgCl2溶液,阳极是氯离子放电生成氯气,阴极是溶液中氢离子放电生成氢气,溶液中氢氧根离子结合镁离子生成氢氧化镁沉淀;
C.乙醛溶液中加入新制碱性Cu(OH)2悬浊液并加热生成红色沉淀氧化亚铜,乙酸钠和水;
D.滴加氨水至过量,得到银氨溶液;
解答 解:A.用铜电极电解CuSO4溶液,离子方程式:Cu+2H20$\frac{\underline{\;通电\;}}{\;}$Cu2++4H++O2↑,故A错误;
B.惰性电极电解MgCl2溶液,阳极是氯离子放电生成氯气,阴极是溶液中氢离子放电生成氢气,溶液中氢氧根离子结合镁离子生成氢氧化镁沉淀,Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Mg(OH)2↓+Cl2↑+H2↑,故B错误;
C.乙醛溶液中加入新制碱性Cu(OH)2悬浊液并加热生成红色沉淀氧化亚铜,乙酸和水,反应离子方程式为:CH3CHO+2 Cu(OH)2+OH-$\stackrel{△}{→}$ CH3COO-+Cu2O↓+3H2O,故C正确;
D.滴加氨水至过量,得到银氨溶液,离子反应为Ag++2NH3•H2O=Ag(NH3)2++2H2O,故答案为:Ag++2NH3•H2O=Ag(NH3)2++2H2O,故D错误;
故选C.
点评 本题考查了电解原理、电解产物判断、物质性质和离子方程式书写等,掌握基础是解题关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将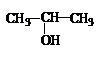 与NaOH的水溶液共热制备CH3-CH═CH2 与NaOH的水溶液共热制备CH3-CH═CH2 | |
| B. | 用甲苯与稀硝酸、稀硫酸的混合酸相混制取TNT | |
| C. | 甲苯在溴化铁催化作用下与液溴反应生成2,4,6-三溴甲苯 | |
| D. | 向CH3CH2Br中滴入AgNO3溶液就可以检验溴元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| PH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氯水中加入Na2CO3粉末有气体产生 | |
| B. | 用强光照射装满次氯酸的试管(倒置于水槽中)可收集到两种气体 | |
| C. | 漂白粉和次氯酸溶液都是混合物 | |
| D. | 向漂白粉中加入浓盐酸可能产生黄绿色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com