
分析 在下列平衡体系中加入盐酸后,若增大反应物的浓度或减少生成物的浓度,则平衡正向移动,若减小反应物的浓度或增大生成物的浓度,则平衡逆向移动,据此分析.
解答 解:(1)HCO3-+H2O?H2CO3+OH-,加盐酸,消耗了OH-,OH-的浓度减小,平衡正向移动;
答:正向移动;加盐酸,减少了生成物的浓度;
(2)Al3++3H2O?Al(OH)3+3H+,加盐酸,H+的浓度增大,平衡逆向移动;
答:逆向移动;加盐酸,增大了生成物的浓度;
(3)S2-+H2O?HS-+OH-加盐酸,消耗了OH-,OH-的浓度减小,平衡正向移动;
答:正向移动;加盐酸,减少了生成物的浓度;
4)CH3COO-+H2O?CH3COOH+OH-,加盐酸,消耗了OH-,OH-的浓度减小,平衡正向移动;
答:正向移动;加盐酸,减少了生成物的浓度.
点评 本题考查了化学平衡移动的影响因素,题目难度不大,侧重于基础知识的考查,注意把握反应物和生成物浓度的影响.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题

| A. | 曲线a是使用了催化剂的能量变化曲线 | |
| B. | 反应物的总键能高于生成物的总键能 | |
| C. | 反应的热化学方程式为:4HCl(g)+O2(g)$→_{400℃}^{催化剂}$2Cl2+2H2O(g)△H=+115.6 kJ/mol | |
| D. | 若反应生成2 mol 液态水,放出的热量高于115.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
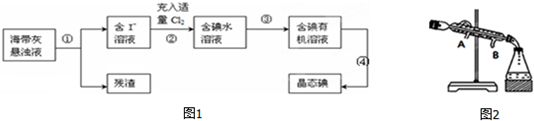
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
 ,硒(Se)是人体必需的微量元素,与⑧同一主族且比⑧原子多一个电子层,则Se的原子序数为34.
,硒(Se)是人体必需的微量元素,与⑧同一主族且比⑧原子多一个电子层,则Se的原子序数为34.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④①②③ | B. | ④②①③ | C. | ②④①③ | D. | ④①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClO3-的空间构型为平面三角形 | |
| B. | SiF4 和 SO32-的中心原子均为 sp3 杂化 | |
| C. | 在所有的元素中,氟的第一电离能最大 | |
| D. | C2H5OH 分子中共含有 8 个极性键,1 个 π 键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com