
以溴乙烷为原料制备1,2-二溴乙烷,下列方案中最合理的是( )
A.CH3CH2Br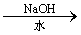 CH3CH2OH
CH3CH2OH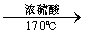 CH2=CH2
CH2=CH2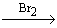 CH2BrCH2Br
CH2BrCH2Br
B.CH3CH2Br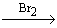 CH2BrCH2Br
CH2BrCH2Br
C.CH3CH2Br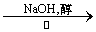 CH2=CH2
CH2=CH2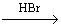 CH2BrCH3
CH2BrCH3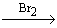 CH2BrCH2Br
CH2BrCH2Br
D.CH3CH2Br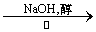 CH2=CH2
CH2=CH2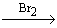 CH2BrCH2Br
CH2BrCH2Br
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
(1)在一次化学晚会上,一位同学表演了一个有趣的魔术:用蘸有饱和硫酸铜溶液的玻璃棒在一洁净的铁片上点上数处,所点之处,点铁成“金”。你知道其中的奥妙吗?请用化学方程式表示其反应原理:
__________________________________________________________________。
(2)铜在自然界多以+1价矿石存在,因为在固态或是高温下+1价铜比+2价铜稳定。辉铜矿(Cu2S)炼铜的方法之一是将矿石高温通空气焙烧,生成两种氧化物。将焙烧过的矿石加上比它质量约少一半的未经焙烧的矿石,混合后隔绝空气再进行高温熔烧,结果得到金属铜和一种具有刺激性气味的气体。这两个反应的化学方程式为 、 。
(3)已知CuS、Cu2S均为黑色不溶于水的固体,在空气中灼烧均生成CuO与SO2,不用其他试剂,设计最简单的实验来鉴别二者: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某温度下,反应SO2(g)+NO2(g)  SO3(g)+NO(g)的平衡常数K=0.24,下列说法正确的是( )
SO3(g)+NO(g)的平衡常数K=0.24,下列说法正确的是( )
A.该温度下反应2SO2(g)+2NO2(g)  2SO3(g)+2NO(g)的平衡常数为0.48
2SO3(g)+2NO(g)的平衡常数为0.48
B.若该反应ΔH<0,则升高温度化学平衡常数K减小
C.若升高温度,逆反应速率减小
D. 改变条件使平衡正向移动,则平衡时n(NO2)/n(NO)一定比原平衡小
查看答案和解析>>
科目:高中化学 来源: 题型:
LED系列产品是被看好的一类节能新产品, 下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是 ( )
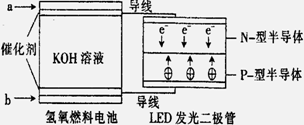
A.a处通入氢气,发生了还原反应: H2-2e-+2OH-=2H2O
B.b处通入氧气,为电池的正极
C.该装置中只涉及两种形式的能量转化,电池中的KOH溶液也可用稀硫酸溶液代替
D.P-型半导体连接的是电池负极
查看答案和解析>>
科目:高中化学 来源: 题型:
中国国家游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成聚全氟乙丙烯。下列说法错误的是( )
A.ETFE分子中可能存在“—CH2—CH2—CF2—CF2—”的连接方式
B.合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应
C.聚全氟乙丙烯分子的结构简式可能为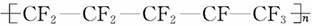
D.聚全氟乙丙烯不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
工业合成UV高级油墨的主要成分的路线图如下:
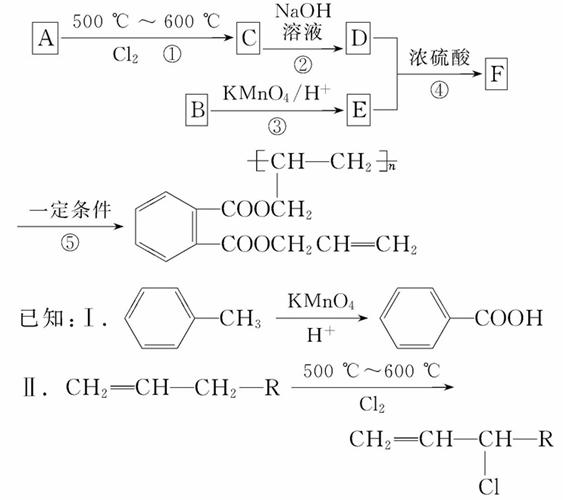
请回答:
(1)A的结构简式为___________________________________________。
(2)下列有关D的说法,正确的是_______(填序号)。
A.能使紫色石蕊试液变红
B.能发生缩聚反应
C.能发生取代反应
D.能发生加成反应
(3)F的官能团有_______种(不含苯环)。1 mol F与氢氧化钠溶液共热,最多能消耗_______mol NaOH。
(4)反应②的化学方程式为_______________________________________。
(5)E有多种同分异构体,写出同时符合以下条件的同分异构体的结构简式_______________________________________。
①与NaHCO3反应能生成CO2气体
②与新制氢氧化铜悬浊液共热能生成红色沉淀
③苯环上的一氯代物只有2种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A.石炭酸与NaOH溶液混合: H+ + OH—  H2O
H2O
B.稀HNO3洗涤试管中的银镜:Ag + NO3— + 2H+ == Ag+ + NO↑ + H2O
C.乙烯使酸性KMnO4褪色:5C2H4 + 12MnO4— + 36H+ 12Mn2++ 10CO2↑ + 28H2O
12Mn2++ 10CO2↑ + 28H2O
D.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:
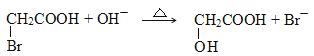
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验设计能够达到目的的是( )
| 编号 | 实验目的 | 实验设计 |
| A | 证明盐酸酸性比醋酸强 | 用同一电路测等体积盐酸、醋酸溶液的导电性 |
| B | 证明H2CO3酸性比H2SiO3强 | 将CO2通入Na2SiO3溶液中 |
| C | 证明钠的金属活动性比铜强 | 向CuCl2溶液中投入金属钠 |
| D | 证明溶液中含有I- | 向溶液中加入淀粉溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com