
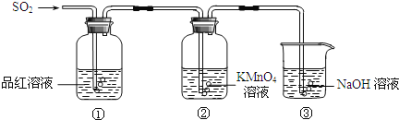
【题目】某研究小组的同学利用如图所示装置探究二氧化硫气体的性质。请回答:
(1)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是____。
(2)当观察到②中溶液颜色变浅时,①中的现象是____。
(3)装置③的作用是___。
(4)①中的现象说明二氧化硫具有的性质是___。
(5)②中的现象说明二氧化硫具有的性质是___。
【答案】Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑ 品红溶液褪色(或变浅) 吸收未反应的二氧化硫,防止污染环境 漂白性 还原性
CuSO4+2H2O+SO2↑ 品红溶液褪色(或变浅) 吸收未反应的二氧化硫,防止污染环境 漂白性 还原性
【解析】
铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫气体和水,二氧化硫具有漂白性,能够使品红溶液褪色反应,二氧化硫有还原性,能使酸性高锰酸钾溶液褪色,二氧化硫有毒,不能直接排放,需要用氢氧化钠溶液吸收。
(1)铜与浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑,故答案为:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,故答案为:Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑;
CuSO4+2H2O+SO2↑;
(2)二氧化硫具有漂白性,将二氧化硫通入品红溶液后,会观察到①中品红溶液褪色(或变浅),故答案为:品红溶液褪色(或变浅);
(3)二氧化硫为有毒气体,多余的二氧化硫不能直接排放,所以装置③中氢氧化钠溶液的作用是吸收未反应的SO2,防止污染环境,故答案为:吸收未反应的SO2,防止污染环境;
(4)二氧化硫具有漂白性,能使品红溶液褪色,装置①中品红溶液褪色,证明二氧化硫具有漂白性,故答案为:漂白性;
(5)二氧化硫具有还原性,酸性高锰酸钾溶液具有强氧化性,二氧化硫能使酸性高锰酸钾溶液褪色,②中酸性高锰酸钾溶液褪色,说明二氧化硫具有还原性,故答案为:还原性。


科目:高中化学 来源: 题型:
【题目】(1)写出下列物质的电子式:
NaCl____________;HCl_____________
(2)第三周期元素中的最高价氧化物对应的水化物中,酸性最强的是________,碱性最强的是_____________,呈两性的氢氧化物是_______________。半径最大的原子是__________,氢化物最稳定的元素是___________。
(3)硫元素位于元素周期表中______周期_______族,气态氢化物的化学式是____________,最高价氧化物对应水化物的化学式_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是( )

A.在图示的转化中,Fe3+和CuS是中间产物
B.在图示的转化中,化合价不变的元素只有铜
C.图示转化的总反应是2H2S+O2![]() 2S+2H2O
2S+2H2O
D.当有1molH2S转化为硫单质时,需要消耗O2的物质的量为0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.![]() 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用,请回答下列问题。
是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用,请回答下列问题。
(1)![]() 属于_____________(填:氧化物,碱,盐)。
属于_____________(填:氧化物,碱,盐)。
(2)浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,原因用离子方程式表示为:______________。(已知酸性:![]() -)
-)
(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是_______。
II.Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知:![]() ,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中被氧化和未被氧化的
,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中被氧化和未被氧化的![]() 的物质的量比_______。
的物质的量比_______。
(5)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
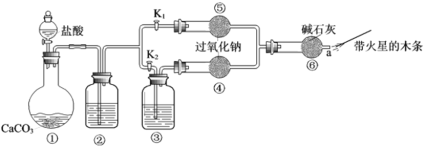
【题目】某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。
(装置分析)
(1)装置①中反应的化学方程式是___________。
(2)装置②中的试剂是___________(填序号)。装置③中的试剂是___________.
a.饱和![]() 溶液 b.饱和
溶液 b.饱和![]() 溶液 c.浓
溶液 c.浓![]()
(进行实验)
步骤1:打开弹簧夹![]() ,关闭
,关闭![]() ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹![]() ,关闭
,关闭![]() ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(3)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是__________;__________。
(4)过氧化钠跟二氧化碳反应的化学方程式是________
(实验反思)
(5)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应。”其理由是_______。
(6)需要补充的实验操作是:取⑤中反应后的少量固体,_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,铝元素能损害人的脑细胞。适当地补充碘元素可预防甲状腺肿大,但摄入过多也会导致甲状腺肿大,因此补充人体所需的元素时也要适可而止。试回答下列问题:
(1)Fe也是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:________。
(2)与Al同一周期的Na、Mg元素也是人体所需元素,Na、Mg、Al基态原子第一电离能的大小关系是________。
(3)氯化铝的熔点是194℃,氧化铝的熔点是2054℃,但是工业上不能用电解熔融氯化铝的方法获取铝单质,这是因为________________________________________。
(4)F与I是同一主族的元素,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别为________、________,BeF2分子的立体构型是________,H2O分子的立体构型是________。
(5)I2晶体的晶胞结构如图所示,该晶胞中含有________个I2分子,设该晶胞的晶胞参数为acm,则I2的密度是________________g·cm-3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
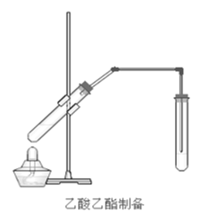
(1)写出制取乙酸乙酯的化学反应方程式________
(2)浓硫酸的作用是:①________;②________。
(3)饱和碳酸钠溶液的主要作用是________、________、________。
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中的目的是防止________。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是________。
(6)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分离出合成气中的H2,用于氢氧燃料电池。如图为电池示意图。
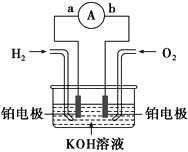
(1)氢氧燃料电池的能量转化主要形式是___,在导线中电子流动方向为___(用a、b和箭头表示)。
(2)正极反应的电极反应方程式为___。
(3)当电池工作时,在KOH溶液中阴离子向___移动(填正极或负极)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】伪麻黄碱(D)是新康泰克的成分之一,能够缓解感冒时带来的鼻塞、流鼻涕和打喷嚏等症状,其中一种合成路线如下:
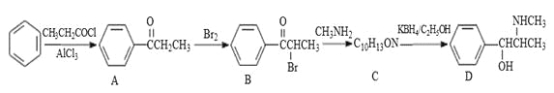
回答下列问题:
(1)伪麻黄碱(D)的分子式为 ;B中含有的官能团有 (写名称)。
(2)写出 B—C反应的化学方程式: 。C—D的反应类型为 。
(3)B的消去产物可以用于合成高分子化合物E,请写出 E的结构简式: 。
(4)满足下列要求的A的同分异构体有 种;
①能发生银镜反应
②苯环上的一氯代物有两种结构,其中核磁共振氢谱为4组峰,且峰面积之比为6:2:1:1的为 (写结构简式)。
(5)已知:![]() 。参照上述合成路线,设计一条由苯和乙酸为起始原料制备
。参照上述合成路线,设计一条由苯和乙酸为起始原料制备![]() 的合成路线: 。
的合成路线: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com