
分析 根据V=$\frac{m}{ρ}$计算出200g乙酸溶液的体积,然后根据n=cV计算出该乙酸溶液中含有乙酸的物质的量,最后根据m=nM计算出该乙酸溶液中含有乙酸的质量.
解答 解:已知该溶液的密度为1.07g/cm3.则200g该乙酸溶液的体积为:$\frac{200g}{1.07g/c{m}^{3}}$=186.91mL≈0.18691L,
该乙酸溶液中含有乙酸的物质的量为:14mol/L×0.18691L=2.61674mol,
所以该溶液中含有乙酸的质量为:60g/mol×2.61674mol≈157.00g,
故答案为:157.00.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、物质的量浓度之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的化学计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲烷在空气中燃烧 | B. | 金属钠与水反应 | ||
| C. | 铝粉与氧化铁粉末反应 | D. | 焦炭在高温下与水蒸气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是周期表中原子序数小于20的9种元素单质的沸点与原子序数的关系,图中原子序数是连续的.试根据如图,回答下列问题:
如图是周期表中原子序数小于20的9种元素单质的沸点与原子序数的关系,图中原子序数是连续的.试根据如图,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
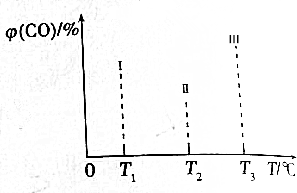
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 选项 | 现象或事实 | 解释 |
| A | 用热的纯碱溶液洗去油污 | Na2CO3可直接与油污反应 |
| B | 常温下,在足量的浓、稀硝酸中分别加入相同的铝片,浓硝酸中铝片先溶解完 | 反应物浓度越大,反应速率越快 |
| C | 用pH计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度 | 乙酸乙酯是非电解质,它不能导电,它的水解产物乙酸是电解质(弱酸) |
| D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含Cu2+的溶液中置换出铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 应称取氢氧化钠固体的质量/g | 应选用容量瓶的规格/mL | 除烧杯、托盘天平、容量瓶、量筒外还需的其它仪器 |
| 10.0 | 250 | 玻璃棒、胶头滴管、药匙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 0.1032mol/LHCl溶液体积/mL | 待测NaOH溶液体积/mL |
| 1 | 27.83 | 25.00 |
| 2 | 25.53 | 25.00 |
| 3 | 27.85 | 25.00 |
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 1.8×10-10 | 5.0×10-13 | 8.3×10-17 | 2.0×10-48 | 1.8×10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | SiCl4 | SiHCl3 | AlCl3 | FeCl3 |
| 沸点/℃ | 57.7 | 33.0 | - | 315 |
| 升华温度/℃ | - | - | 180 | 300 |
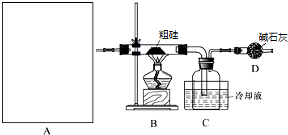
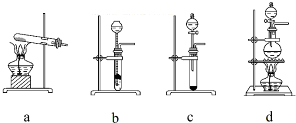
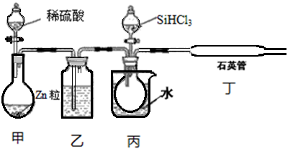
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当△H为“-”时,表示该反应为吸热反应 | |
| B. | 等量H2在O2中完全燃烧,生成H2O(g)与生成H2O(1)放出的能量相同 | |
| C. | 反应热的大小与反应物所具有的能量和生成物所具有的能量无关 | |
| D. | 化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com