
| A、用25mL的碱式滴定管量取14.80mL的酸性KMnO4溶液 |
| B、用100mL容量瓶配制80mL 0.1mol?L-1的盐酸 |
| C、用pH试纸测得醋酸的pH为3.20 |
| D、用10mL量筒量取5.2mL盐酸 |
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
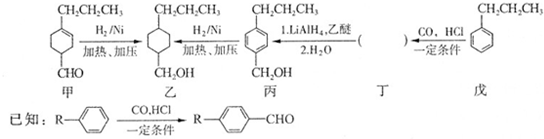
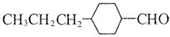 和
和查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
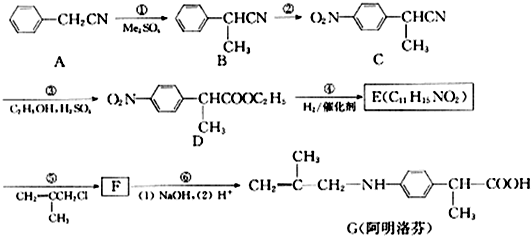
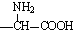 ②含有对位二取代苯环
②含有对位二取代苯环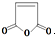 是合成某些药物的中间体.试设计合理方案由化合物
是合成某些药物的中间体.试设计合理方案由化合物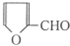 合成
合成 .
. 在400℃有金属氧化物存在条件下能发生脱羰基(
在400℃有金属氧化物存在条件下能发生脱羰基(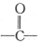 )反应.
)反应.| 反应物 |
| 反应条件 |
| 反应物 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、14.3% | B、12.5% |
| C、87.5% | D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.
短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.查看答案和解析>>
科目:高中化学 来源: 题型:
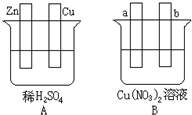 按要求对如图中两极进行必要的联接并填空,a、b为惰性材料.
按要求对如图中两极进行必要的联接并填空,a、b为惰性材料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com