
| A、实验室用NH4Cl和Ca(OH)2制备NH3 | B、工业上电解熔融状态的Al2O3制备Al | C、工业上利用合成氨实现人工固氮 | D、Na2O2用作呼吸面具的供氧剂 |
| ||
| ||


科目:高中化学 来源: 题型:
| A、1 mol羟基(-OH)所含的电子数约为10NA | B、标准状况下,22.4 L甲醇中含有的氧原子数为1.0NA | C、25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.1NA | D、53.5gNH4Cl中含有H-Cl键的个数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁与足量稀硝酸反应,1mol Fe失去电子数为3NA | B、常温常压下,22.4L乙烯中含极性共价键数目为3NA | C、1L 1mol?L-1的NH4Cl溶液中有NA个NH4+ | D、1mol冰醋酸和lmol乙醇在浓硫酸加热下充分反应生成H2O个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、标准状况下,1,12 L氡气(
| ||
| B、7.8 g Na2S和Na2O2混合物中含有的阴、阳离子总数是0.3NA | ||
| C、某温度时1 L pH=6的纯水所含OH-数目为1.0×10-6NA | ||
| D、用惰性电极电解1L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2NA个电子转移时,理论上阴极析出6.4 g金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 0.1mol?L-1的CuCl2溶液中含Cu2+为0.1NA | B、标准状况下,22.4L CCl4含CCl4分子为NA | C、1mol H3O+含质子数为10NA | D、1mol Na2O和Na2O2混合物中含阴离子的总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合物溶解后的溶液中c(Fe3+):c(Fe2+)=1:l | B、需加入NaOH溶液1000mL | C、稀硝酸的物质的量浓度是2mol?L-1 | D、最后所得沉淀在空气中充分加热可得固体32g |
查看答案和解析>>
科目:高中化学 来源: 题型:
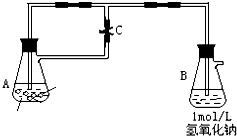 图中为制取纯净且能较长时间存在的Fe(OH)2,药品为铁粉、稀H2SO4,NaOH溶液,当容器A中反应开始后,若分别进行下列操作,请回答有关问题:
图中为制取纯净且能较长时间存在的Fe(OH)2,药品为铁粉、稀H2SO4,NaOH溶液,当容器A中反应开始后,若分别进行下列操作,请回答有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2、CH4等均为能造成温室效应的气体 | B、工业上大量燃烧含硫的燃料和金属矿石的冶炼是造成酸雨的主要原因 | C、明矾可用于水的消毒,杀菌 | D、合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com