
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A. 17 g羟基(—OH)所含有的电子数是10NA个
B. 1 mol苯乙烯中含有的碳碳双键数为4NA个
C. 常温下,14 g乙烯和丙烯的混合物中总原子数为3NA个
D. 4.2 g C3H6中含有的碳碳双键数一定为0.1NA
科目:高中化学 来源: 题型:
【题目】(1)碳化硅(SiC)是一种晶体,具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。下列各种晶体:①晶体硅 ②硝酸钾 ③金刚石 ④碳化硅 ⑤干冰 ⑥冰,它们的熔点由高到低的顺序是___________(填序号)。
(2)下列离子晶体的立体构型示意图,如下图所示。
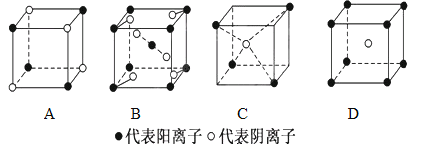
以M代表阳离子,以N代表阴离子,写出各离子晶体的组成表达式。
A.__________,B:________,C:________,D:_____________。
(3)已知FeS2晶体(黄铁矿的主要成分)具有A的立体结构。
①FeS2晶体中具有的化学键类型是______________。
②若晶体结构A中相邻的阴、阳离子间的距离为acm,且用NA代表阿伏加德罗常数,则FeS2晶体的密度是________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
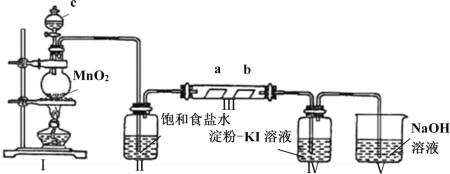
(1)装置Ⅰ中仪器c的名称是_______________,实验室以二氧化锰和浓盐酸制备氯气的离子方程式为_______________________________________________________。
(2)装置Ⅱ的作用是________________________。
(3)实验过程中装置Ⅳ中的实验现象为______________________________。
(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与III之间添加下图中的_______装置(填序号)。

(5)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有德国重离子研宄中心人工合成的第112号元素的正式名称为“Copemicium”,相应的元素符号位“Cn”,该元素的名称是为了纪念天文学家哥白尼而得名。该中心人工合成Cn的过程可表示为:
![]() 。下列叙述中正确的是
。下列叙述中正确的是
A. 上述合成过程中属于化学变化
B. Cn元素的相对原子质量为277
C. ![]() 的原子核内中子数比质子数多53
的原子核内中子数比质子数多53
D. Cn元素位于元素周期表的第六周期,是副族元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) TiO2是一种性能优良的半导体光催化剂,能有效地吸附有机污染物,Ti基态核外电子排布式为________________。
(2)甲醛HCHO分子空间构型为_____;分子中碳原子轨道杂化类型为_____,π键和σ键的个数之比为____,
(3)SO2易溶于水的原因是___________________________________。
(4)从原子结构角度解释H2SO4酸性强于H3PO4的原因:___________________________。
(5)含CN-的污水毒性极大,用NaClO先把CN-氧化为CNO-,然后在酸性条件下将CNO-氧化为无污染的气体。请写出与CNO-互为等电子体的微粒______(分子或离子,写一种)。
(6)下列物质在通常状况下的熔点由高到低的顺序为__________(填序号)
①CO ②Al2O3③NH3 ④N2⑤Br2
(7)不考虑空间构型,Ti[(CN)4]2-的结构可表示为:_____________________。
(8)向硫酸铜溶液中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,请根据实验现象写出有关反应的离子方程式 (1)____________________________(2)_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2甲基丁烷。若将化合物X用NaOH的水溶液处理,则所得有机产物的结构简式可能是( )
A.CH3CH2CH2CH2CH2OH B.(CH3)2COHCH2CH3
C.(CH3)2CHCH2CH2OH D.(CH3)3CCH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁的电化学腐蚀原理如图所示,下列有关说法中错误的是( )
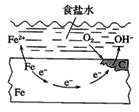
A. 铁片里的铁和碳与食盐水形成无数的微小原电池
B. 铁电极发生氧化反应
C. 负极的电极反应方程式为O2+4e-+2H2O=4OH-
D. 放置一段时间后,铁片上有铁锈出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述中正确的是( )
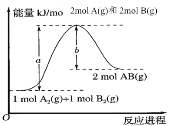
A.该反应需要在加热条件下才能进行
B.每生成2mol AB(g)吸收的热量为(a—b)kJ
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1mol A—A键和1mol B—B键,放出a kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸中的一步重要反应是SO2在400-500℃和常压下的催化氧化: 2SO2 + O2![]() 2SO3, 这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述相关说法中错误的是
2SO3, 这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述相关说法中错误的是
A.反应温度选择400-500℃是该反应催化剂的催化活性、反应速率、反应限度等角度综合考虑的结果
B.因为在常压下该反应的速率和SO2的转化率已经很高了,所以选择常压条件主要是从生产成本角度考虑
C.为提高SO2的转化率,应适当提高O2的浓度
D.使用催化剂是为了加快反应速率,提高SO3产率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com