
【题目】工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取二氧化锰,其流程示意图如下: 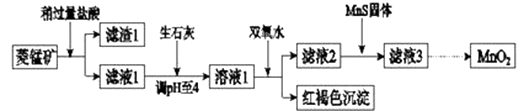
已知:生成氢氧化物沉淀的pH
Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
注:金属离子的起始浓度为0.1mol/L,回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是 . 盐酸溶解MnCO3的化学方程式是 .
(2)向溶液1中加入双氧水时,反应的离子方程式是 .
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+ , 反应的离子方程式是 .
(4)将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:Mn2++ClO3﹣+=++ .
(5)将MnCl2转化为MnO2的另一种方法是电解法.
①阳极生成MnO2的电极反应式是 .
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2 . 检验Cl2的操作是 .
③若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生.其原因是 .
【答案】
(1)增大接触面积,提高反应速率;MnCO3+2HCl=MnCl2+CO2↑+H2O
(2)2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+
(3)MnS+Cu2+=Mn2++CuS
(4)5;2;4H2O;1Cl2↑;5MnO2;8H+???
(5)Mn2+﹣2e﹣+2H2O=MnO2+4H+;将润湿的淀粉碘化钾试纸置于阳极附近,若试纸变蓝则证明有Cl2生成;其它条件不变下,增大Mn2+浓度或增大 ![]() ,有利于Mn2+放电(不利于Cl﹣放电)
,有利于Mn2+放电(不利于Cl﹣放电)
【解析】解:菱锰矿用盐酸酸浸,MnCO3、FeCO3、Cu2(OH)2CO3与盐酸反应,SiO2不与盐酸反应,过滤得到滤渣1为SiO2 , 滤液1中含有氯化镁、氯化亚铁、氯化铜及剩余的HCl,向滤液中加入生石灰,调节溶液pH=4,加入过氧化氢将溶液中Fe2+氧化为Fe3+ , 在PH=4时氧化得到Fe3+转化为Fe(OH)3沉淀,过滤除去,滤液2中加入MnS,将溶液中Cu2+转化为CuS沉淀过滤除去,滤液3中为MnCl2 , 系列转化得到MnO2 .
(1.)将菱锰矿粉碎,可以增大接触面积,提高反应速率;碳酸镁与盐酸反应生成氯化镁、二氧化碳与水,反应方程式为:MnCO3+2HCl=MnCl2+CO2↑+H2O,所以答案是:增大接触面积,提高反应速率;MnCO3+2HCl=MnCl2+CO2↑+H2O;
(2.)加入过氧化氢将溶液中Fe2+氧化为Fe3+ , 在PH=4时氧化得到Fe3+转化为Fe(OH)3沉淀,根据电荷守恒有氢离子生成,反应离子方程式为:2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+ , 所以答案是:2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+;
(3.)MnS与氯化铜反应转化更难溶的CuS,同时得到氯化镁,反应离子方程式为:MnS+Cu2+=Mn2++CuS,所以答案是:MnS+Cu2+=Mn2++CuS;
(4.)用酸化的NaClO3溶液将MnCl2氧化得到MnO2 , Mn元素发生氧化反应,则Cl元素发生还原反应生成Cl2 , 由于在酸性条件下反应,根据电荷守恒可知,生成物中有H+生成,根据H元素守恒,可知反应物中缺项物质为H2O,配平后离子方程式为:5Mn2++2ClO3﹣+4H2O=Cl2↑+5MnO2+8H+ , 所以答案是:5,2,4H2O,1Cl2↑,5MnO2 , 8H+;
(5.)①由题意可知,Mn2+转化为MnO2 , 发生氧化反应,由O元素守恒可知有水参加反应,由电荷守恒可知应有H+生成,电极反应式为:Mn2+﹣2e﹣+2H2O=MnO2+4H+ , 所以答案是:Mn2+﹣2e﹣+2H2O=MnO2+4H+;②生成氯气发生氧化反应,在阳极产生,检验Cl2的操作是:将润湿的淀粉碘化钾试纸置于阳极附近,若试纸变蓝则证明有Cl2生成,所以答案是:将润湿的淀粉碘化钾试纸置于阳极附近,若试纸变蓝则证明有Cl2生成;③Mn2+、Cl﹣都在阳极放电,二者为竞争关系,增大Mn2+浓度或增大 ![]() ,有利于Mn2+放电(不利于Cl﹣放电),所以答案是:其它条件不变下,增大Mn2+浓度或增大
,有利于Mn2+放电(不利于Cl﹣放电),所以答案是:其它条件不变下,增大Mn2+浓度或增大 ![]() ,有利于Mn2+放电(不利于Cl﹣放电).
,有利于Mn2+放电(不利于Cl﹣放电).


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】某可充电的锂离子电池,以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池总反应为:Li+LiMn2O4=Li2Mn2O4。下列说法正确的是
A.放电时,LiMn2O4发生氧化反应
B.放电时,正极反应为:Li++LiMn2O4+e- =Li2Mn2O4
C.充电时,LiMn2O4发生氧化反应
D.充电时,阳极反应为:Li++e- =Li
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,海水的综合利用具有重要意义(如下图)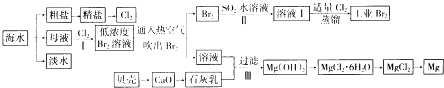
(1)氯碱工业主要以食盐为原料,为了除去粗盐中的Ca2+、Mg2+、SO42﹣及泥沙,可将粗盐溶于水,然后进行下列操作:①加过量的NaOH溶液;②加过量的BaCl2溶液③加过量的Na2CO3溶液;④过滤;⑤加适量的盐酸,第③步操作的目的是
(2)在实验室可以用萃取的方法提取溴,在萃取操作过程中,下列说法不正确的是 .
A.萃取剂可选用苯、CCl4、裂化汽油等有机溶剂.
B.萃取分液时下层液体从下口放出,上层液体从上口倒出
C.在萃取过程中,需要振荡分液漏斗,并打开分液漏斗上口的玻璃塞放气.
(3)通入热空气吹出溴,并用SO2的水溶液吸收的目的是 .
(4)步骤Ⅰ中用硫酸酸化可提高Cl2利用率的原因是 .
(5)步骤Ⅲ中有关反应的离子方程式 , 解释该反应能够发生的原因 .
(6)海水提溴蒸馏过程中,温度应控制在80﹣90℃,温度过高或过低都不利于生产,请解释原因 .
(7)工业上不用电解熔融MgO制金属镁,理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列检验方法与结论相符的一组是( )
序号 | 检 验 方 法 | 结 论 |
A | 向一种未知溶液中滴加AgNO3溶液,有白色沉淀 | 未知溶液中一定含有Cl﹣ |
B | 向一种未知溶液中滴加盐酸,有气泡产生 | 未知溶液中一定含有CO |
C | 将一种未知气体通入品红溶液,溶液褪色,加热后又恢复红色 | 未知气体是SO2 |
D | 向一种未知溶液中滴加BaCl2溶液,有白色沉淀 | 未知溶液中一定含有SO |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学实验操作中必须注意安全操作,下列操作或事故处理正确的是( ) ①在点燃易燃性气体前,必须检验气体的纯度
②在稀释浓硫酸时应将浓硫酸沿器壁慢慢注入水中,并用玻璃棒搅拌
③浓硫酸对皮肤有腐蚀性,如不慎沾到皮肤上,应用较多的水冲洗,再涂上硼酸液
④给试管中的液体加热时,液体体积不超过试管容积的三分之一
⑤点燃盛满酒精的酒精灯.
A.仅①②
B.仅①②③
C.仅①②④
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间的转化在给定条件下不能实现的是( )
A.Al2O3 ![]() NaAlO2(aq)
NaAlO2(aq) ![]() Al(OH)3
Al(OH)3
B.S ![]() SO3
SO3 ![]() H2SO4
H2SO4
C.饱和NaCl(aq) ![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
D.MgCl2(aq) ![]() Mg(OH)2
Mg(OH)2 ![]() MgO
MgO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com