
| A、某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他现象,说明该溶液中一定含有SO42- |
| B、某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有 CO32-或 HCO3- |
| C、某溶液中加盐酸产生刺激性气味的无色气体,该气体能使品红溶液褪色,说明该溶液中一定含有SO32- |
| D、取少量久置的Na2SO3样品于试管中加水溶解,再加入足量盐酸有气体产生,然后加入BaCl2溶液有白色沉淀产生,说明Na2SO3样品已部分被氧化 |


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
| A、植物油可以作为萃取剂分离出碘水中的碘 |
| B、石油的分馏、煤的气化、海水制镁都包括化学变化 |
| C、处理废水时加入明矾作为消毒剂,可以除去水中的杂质 |
| D、乙烯、甲烷、SO2三种无色气体可用溴水鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、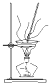 灼烧 |
B、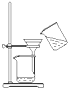 过滤 |
C、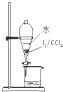 分液 |
D、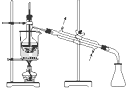 蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、Cl-、CO32- |
| B、K+、Na+、NO3-、SO42- |
| C、Mg2+、K+、NO3-、Cl- |
| D、Fe2+、NO3-、SO42-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
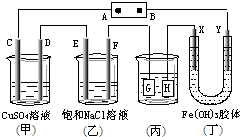 如图,C、D,E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色.则下列说法正确的是( )
如图,C、D,E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色.则下列说法正确的是( )| A、若用乙烷、空气燃料电池作电源,电解质为KOH溶液,则B极的电极反应式为:02+2H20+4e-=40H- |
| B、欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 |
| C、(丁)装置中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷 |
| D、C、D、E、F电极均有单质生成,其物质的量比为1:2:2:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、气体甲中SO2与H2的体积比为4:1 |
| B、反应中共消耗1.8 mol H2SO4 |
| C、反应中共消耗97.5 g Zn |
| D、反应中共转移3 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PH之和等于14的HNO3与KOH溶液 |
| B、PH之和等于14的盐酸与氨水 |
| C、PH之和等于15的H2SO4和NaOH溶液 |
| D、PH之和等于14的CH3COOH和Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加压(体积变小),将使正逆反应速率均加快 |
| B、保持体积不变,加入少许NO2,将使正反应速率减小 |
| C、保持体积不变,加入少许N2O4,再达平衡时,颜色变深 |
| D、保持体积不变,升高温度,再达平衡时,颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
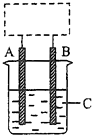 某学生设计了如图所示的装置(框内部分未画出),在装置内起初发生的反应为Cu+2HCl=H2↑+CuCl2,请回答:
某学生设计了如图所示的装置(框内部分未画出),在装置内起初发生的反应为Cu+2HCl=H2↑+CuCl2,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com