
 X��Y��Z��W��A����Ԫ�أ���λ�����ڱ���ǰ�����ڣ����ǵĺ˵�����������ӣ��Һ˵����֮��Ϊ57��Yԭ�ӵ�L��p�������2�����ӣ�Z��ԭ�Ӻ���������δ�ɶԵ��ӣ�W��Yԭ�ӵļ۵�������ͬ��Aԭ�ӵ����������������ڲ��������һ�룬��d�������ȫ����״̬��
X��Y��Z��W��A����Ԫ�أ���λ�����ڱ���ǰ�����ڣ����ǵĺ˵�����������ӣ��Һ˵����֮��Ϊ57��Yԭ�ӵ�L��p�������2�����ӣ�Z��ԭ�Ӻ���������δ�ɶԵ��ӣ�W��Yԭ�ӵļ۵�������ͬ��Aԭ�ӵ����������������ڲ��������һ�룬��d�������ȫ����״̬��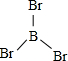 ��
��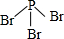 ��
������ X��Y��Z��W��A����Ԫ�أ���λ�����ڱ���ǰ�����ڣ����ǵĺ˵�����������ӣ��Һ˵����֮��Ϊ57��Yԭ�ӵ�L��p�������2�����ӣ�����������Ų�ʽΪ1s22s22p2����YΪCԪ�أ�Aԭ�ӵ����������������ڲ��������һ�룬��d�������ȫ����״̬�����������Ϊ2+8+18+1=29����AΪCu��W��Yԭ�ӵļ۵�������ͬ������ͬ���ڣ�Wԭ������С��Cu����W��Si��Z��ԭ�Ӻ���������δ�ɶԵ��ӣ�ԭ����������̼��С��Si����ZΪNԪ�أ�Xԭ�Ӻ˵����=57-6-7-14-29=1����X��HԪ�أ�
��1��A2+ΪCu2+��Cuԭ��ʧȥ4s�ܼ�1����3d�ܼ�1�������γ�Cu2+��
��2��H��C��N �����γɻ�ѧʽΪHCN�ķ��ӣ��÷����и�ԭ�Ӿ��ﵽϡ�������ȶ��ṹ����÷��ӽṹʽΪH-C��N��
��3��̼��һ���������뵪��һ�������ﻥΪ�ȵ����壬Ӧ��CO2��N2O��
X��Z�γɵ��������QΪNH3��Cu2+��NH3�γɵ������ӵ�����ΪCu��NH3��42+��
��4����BBr3����ԭ�ӵļ۲���Ӷ���Ϊ3+$\frac{3-1��3}{2}$=3��û�йµ��Ӷԣ����Է��ӿռ乹��Ϊƽ�������Σ�PBr3����ԭ�ӵļ۲���Ӷ���Ϊ3+$\frac{5-1��3}{2}$=4��Pԭ����һ�Թµ��Ӷԣ����Է��ӿռ乹��Ϊ�����Σ�
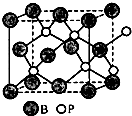
���ɾ����ṹ��֪����BP������B�Ķѻ���ʽΪ���������ܶѻ���
��Pԭ������Χ��4��Bԭ��������γ���������ṹ���������ߴ�����Խ����ϣ���������ԭ�Ӻ���ԭ��֮����������Ϊ��Խ��ߵ�$\frac{1}{4}$������Խ��߳��ȵ��ھ����ⳤ��$\sqrt{3}$����
��� �⣺X��Y��Z��W��A����Ԫ�أ���λ�����ڱ���ǰ�����ڣ����ǵĺ˵�����������ӣ��Һ˵����֮��Ϊ57��Yԭ�ӵ�L��p�������2�����ӣ�����������Ų�ʽΪ1s22s22p2����YΪCԪ�أ�Aԭ�ӵ����������������ڲ��������һ�룬��d�������ȫ����״̬�����������Ϊ2+8+18+1=29����AΪCu��W��Yԭ�ӵļ۵�������ͬ������ͬ���ڣ�Wԭ������С��Cu����W��Si��Z��ԭ�Ӻ���������δ�ɶԵ��ӣ�ԭ����������̼��С��Si����ZΪNԪ�أ�Xԭ�Ӻ˵����=57-6-7-14-29=1����X��HԪ�أ�
��1��A2+ΪCu2+��Cuԭ��ʧȥ4s�ܼ�1����3d�ܼ�1�������γ�Cu2+��Cu2+����Χ�����Ų�ʽΪ3d9��
�ʴ�Ϊ��3d9��
��2��H��C��N �����γɻ�ѧʽΪHCN�ķ��ӣ��÷����и�ԭ�Ӿ��ﵽϡ�������ȶ��ṹ����÷��ӽṹʽΪH-C��N����÷�����Cԭ�Ӽ۲���ӶԸ�����2�Ҳ����µ��Ӷԣ�Cԭ�Ӳ�ȡ���ӻ���ʽΪsp��
�ʴ�Ϊ��sp��
��3��̼��һ���������뵪��һ�������ﻥΪ�ȵ����壬Ӧ��CO2��N2O����Z��������������ΪN2O��
X��Z�γɵ��������QΪNH3��Cu2+��NH3�γɵ������ӵ����ӷ���ʽΪ��Cu2++4NH3�TCu��NH3��42+��
�ʴ�Ϊ��N2O��Cu2++4NH3�TCu��NH3��42+��
ΪCu��NH3��42+��
��4����BBr3����ԭ�ӵļ۲���Ӷ���Ϊ3+$\frac{3-1��3}{2}$=3��û�йµ��Ӷԣ����Է��ӿռ乹��Ϊƽ�������Σ��ṹʽΪ ��PBr3����ԭ�ӵļ۲���Ӷ���Ϊ3+$\frac{5-1��3}{2}$=4��Pԭ����һ�Թµ��Ӷԣ����Է��ӿռ乹��Ϊ�����Σ��ṹʽΪ��
��PBr3����ԭ�ӵļ۲���Ӷ���Ϊ3+$\frac{5-1��3}{2}$=4��Pԭ����һ�Թµ��Ӷԣ����Է��ӿռ乹��Ϊ�����Σ��ṹʽΪ��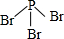 ��
��
�ʴ�Ϊ�� ��
��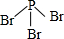 ��
��
���ɾ����ṹ��֪��Bԭ�Ӵ��ھ������������ģ���BP������B�Ķѻ���ʽΪ���������ܶѻ���
�ʴ�Ϊ�����������ܶѻ���
��Pԭ������Χ��4��Bԭ��������γ���������ṹ���������ߴ�����Խ����ϣ�Ϊ��Խ��ߵ�$\frac{1}{4}$���������ÿ���߳�Ϊ478pm������Խ��߳�Ϊ$\sqrt{3}$��478 pm����Pԭ����Bԭ���������Ϊ$\sqrt{3}$��478 pm��$\frac{1}{4}$=$\frac{239\sqrt{3}}{2}$pm��
�ʴ�Ϊ��$\frac{239\sqrt{3}}{2}$pm��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰��������Ų����ӻ���ʽ�жϡ��ȵ����塢���������ṹ�����ȣ���4���о�����ԭ�Ӿ������Ϊ�״��㡢�ѵ㣬��Ҫѧ���߱�һ���Ŀռ���������ѧ�����������Ѷ��еȣ�


 ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д� һ��һ��һ��ͨϵ�д�
һ��һ��һ��ͨϵ�д� �㽭֮��ѧҵˮƽ����ϵ�д�
�㽭֮��ѧҵˮƽ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ�м����������ữ�Ĺ���������Һ��Fe2++2H++H2O2�TFe3++2H2O | |
| B�� | ��֪ͬ�¶��µ��ܽ�ȣ�Zn��OH��2��ZnS��Na2S��Һ��ZnCl2��Һ��ϣ�Zn2++S2-+2H2O�TZn��OH��2��+H2S�� | |
| C�� | 0.01 mol•L-1NH4Al��SO4��2��Һ��0.02 mol•L-1 Ba��OH��2��Һ�������ϣ�Al3++2SO42-+2Ba2++4OH-�T2BaSO4��+AlO2-+2H2O | |
| D�� | ��KI-������Һ�м���ϡ���ᣬ�ڿ����з���һ��ʱ�����Һ����ɫ��4H++4I-+O2�T2I2+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ʵ������ | ���� |
| A | ��NaBr��Һ�м�����ˮ���ټ������KI��Һ | ��Һ���� | �����ԣ�Cl2��Br2��I2 |
| B | ����Ƭ���������� | �������ݵ����ʿ�ʼ���������ӿ죬���������� | H+��Ũ����Ӱ�췴Ӧ���ʵ�Ψһ���� |
| C | ��������Һ�м���ϡ���ᣬˮԡ���Ⱥ�������������ͭ����Һ������ | �õ���ɫ��Һ | ����ˮ�����û�л�ԭ�� ������δˮ�� |
| D | ��Ư���е���ϡ���ᣬ�����ɵ�����ͨ��Ʒ����Һ | Ʒ����Һ��ɫ | �����к���Cl2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol•L-1���Ȼ�����Һ�У���Fe3+����ĿΪ NA����Cl-����ĿΪ3NA | |
| B�� | �����£�1 mol Fe������ϡHNO3��Ӧ��ת�Ƶ��ӵ���ĿΪ2 NA | |
| C�� | 8.0gCu2S��CuO�Ļ�����к��е�ͭԭ����Ϊ0.1NA | |
| D�� | ��״���£�2.24 LCl2����ˮ��ת�Ƶ��ӵ���ĿΪ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
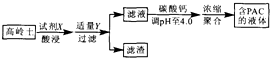 ���ø���������Ҫ�ɷ�ΪA12 O3��SiO2��Fe2O3��Ϊԭ���Ʊ�ˮ�ʾ�����PAC{[A12��OH��nC16-n]m��n��6��mΪ�ۺ϶ȣ�}�Ĺ�����ͼ������˵����ȷ���ǣ�������
���ø���������Ҫ�ɷ�ΪA12 O3��SiO2��Fe2O3��Ϊԭ���Ʊ�ˮ�ʾ�����PAC{[A12��OH��nC16-n]m��n��6��mΪ�ۺ϶ȣ�}�Ĺ�����ͼ������˵����ȷ���ǣ�������| A�� | �Լ�XΪH2SO4 | B�� | ������Ҫ�ɷ�ΪFe��OH��3��H2 SiO3 | ||
| C�� | ��pH������;������PAC���� | D�� | ��ҺŨ���ۺϹ��̷����˼Ӿ۷�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
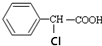 �ж���ͬ���칹�壬����������������ԭ��ֱ�����ڱ����ϵ�ͬ���칹���ж����֣������������칹����������
�ж���ͬ���칹�壬����������������ԭ��ֱ�����ڱ����ϵ�ͬ���칹���ж����֣������������칹����������| A�� | 6�� | B�� | 9�� | C�� | 15�� | D�� | 19�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com