
化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是( )
A.棉花、蚕丝和人造丝的主要成分都是纤维素
B.二氧化硫的排放是造成光化学烟雾的主要因素
C.雨水样品一段时间后,pH由4.68变为4.28,是因为雨水中溶解了较多的氮氧化物和CO2[
D.“毒奶粉”中含有的三聚氰胺(C3H6N6)属有机物,其含氮量远高于奶粉的含氮量
 作业辅导系列答案
作业辅导系列答案科目:高中化学 来源:2016-2017学年广东省高一上期中化学卷(解析版) 题型:实验题
四只试剂瓶中分别盛装有NaNO3 溶液、Na2CO3 溶液、Na2SO4 溶液和NaCl溶液,就如何检验这四种溶液分别解答下列各题。在四支试管中分别取四种溶液各1 mL(只取一次溶液),做下列实验。
(1)在四支试管中分别滴入(写化学式,下同) ,可检验出的物质是 ,离子方程式是 。
(2)在剩余三支试管中分别滴入 ,可检验出的物质是 ,离子方程式是 。
(3)在剩余两支试管中分别滴入 ,可检验出的物质是 , 离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上期中化学试卷(解析版) 题型:填空题
(1)实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷,石墨,氢气燃烧的反应热:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3kJ/mol
C(石墨)+O2(g)=CO2(g) ΔH2=―393.5kJ/mol
H2(g)+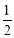 O2(g)=H2O(l) ΔH3=―285.8kJ/mol,则由石墨生成甲烷的反应热:
O2(g)=H2O(l) ΔH3=―285.8kJ/mol,则由石墨生成甲烷的反应热:
C(石墨)+2H2(g)=CH4(g) ΔH 4= 。
(2)体积相同,pH均等于1的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m________n(填>、<、= )
(3)取浓度相等的NaOH和HCl溶液,以3∶2体积比相混和,所得溶液的pH等于12,则原溶液的浓度为_________________
(4) 常温下,某一元酸HA的Ka=2×10-5,则0.05 mol/L该酸溶液的PH值=_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上期中化学试卷(解析版) 题型:选择题
下列变化属于吸热反应的是 ①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰
A、①④⑤ B、①②④ C、②③ D、②④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上阶段考二文化学卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A. 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B. 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C. MgO的熔点很高,可用于制作耐高温材料
D. 光导纤维属于硅酸盐产品[
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上阶段考二文化学卷(解析版) 题型:选择题
下列有关环境保护的说法中错误的是( )
A.含氮、磷化合物的生活污水大量排放可使水体富营养化
B.各国工业大量排放二氧化硫是全球气候变暖的主要原因
C.劣质装修材料中的甲醛、苯、氡气等对人体有害
D.废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:填空题
25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 mol·L-1 | K1=4.4×10-7 mol·L-1 K2=5.6×10-11 mol·L-1- | 3.0×10-8mol·L-1 |
请回答下列问题:
(1)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为________________。
(2)常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填字母序号,下同)。
A.c(H+)
B.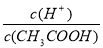
C.c(H+)·c(OH-)
D.
E.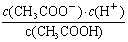
若该溶液升高温度,上述5种表达式的数据增大的是___________。
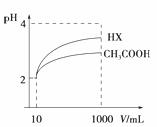
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数__________(填“大于”、“等于”或“小于”)醋酸的平衡常数。稀释后,HX溶液中由水电离出来的c(H+) __________(填“大于”、“等于”或“小于”)醋酸的溶液中由水电离出来的c(H+),理由是______________________________。
(4)已知100℃时,水的离子积为1×10-12,该温度下测得某溶液pH=7,该溶液显__________(填“酸”、“碱”或“中”)性。将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a:b=__________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol 下列结论正确的是
A.碳的燃烧热等于110.5kJ/mol
B.2molC(s)在2molO2(g)燃烧, 放出221kJ热量
C.1L 0.1mol/L硫酸溶液与1L pH=11的NaOH溶液反应,放出5.73kJ热量
D.pH=3的醋酸与pH=11的NaOH溶液反应生成1mol水,放出57.3kJ热量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上期中化学卷(解析版) 题型:选择题
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
从以上表格中判断以下说法中不正确的是
A.在冰醋酸中硫酸的电离方程式为H2SO4===2H++S O
O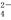
B.在冰醋酸中高氯酸是这四种酸中最强的酸
C.在冰醋酸中这四种酸都没有完全电离
D.水对于这四种 酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com