
【题目】在相同条件下,2mol C燃烧生成2mol CO放出的热量为Q1 , 2mol C 燃烧生成2mol CO2放出的热量为Q2 , Q1和Q2的关系是( )
A.Q1=Q2
B.Q1>Q2
C.Q1<Q2
D.无法确定
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是
A. SO2、SiO2、CO均为酸性氧化物 B. 稀豆浆、硅酸、氯化铁溶液均为胶体
C. 烧碱、冰醋酸、蔗糖均为电解质 D. 盐水、水玻璃、氨水均为混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个体积恒定的密闭容器中,加入2 mol A和1 mol B发生反应:2A(g)+B(g)![]() 3C(g)+D(g),一定条件下达到平衡时,C的浓度为W mol·L1,若容器体积和温度保持不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为W mol·L1的是
3C(g)+D(g),一定条件下达到平衡时,C的浓度为W mol·L1,若容器体积和温度保持不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为W mol·L1的是
A.4 mol A+2 mol B
B.3 mol C+1 mol D
C.2 mol A+1 mol B+3 mol C+1 mol D
D.1 mol A+0.5 mol B+3 mol C+1 mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是一种新型香料的主要成分之一,其结构中含有三个六元环。G的合成路线如下(部分产物和部分反应条件略去):

已知:
①B中核磁共振氢谱图显示分子中有6种不同环境的氢原子;
②D和F互为同系物。
请回答下列问题:
(1)(CH3)2C=CH2的系统命名法名称为 ,生成B这一步的反应类型为 。
(2)E的结构简式为 ,F分子中含有的含氧官能团名称是 。
(3)C经氧化后可得到一种能与新制银氨溶液发生银镜反应的物质,请写出该银镜反应的化学方程式 。
(4)F可在一定条件下合成高分子化合物,请写出该高分子化合物的结构简式 。
(5)同时满足下列条件:①与FeCl3溶液发生显色反应;②苯环上有两个取代基;③能与碳酸氢钠溶液反应放出气体;这样的D的同分异构体共有 种(不包括立体异构);
(6)请参照合成路线中苯乙烯合成F的方法,写出由1-丁烯制取2-羟基丁酸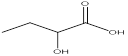 的合成线路: 。
的合成线路: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)![]() 2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素R的原子序数是15,下列关于R元素的说法中,错误的是( )
A. R的最高正化合价是+5
B. R是第2周期第ⅤA族的元素
C. R的氢化物分子式是RH3
D. R的最高价氧化物对应的水化物的水溶液呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据路透社北京报道,中国石油计划2017年加大在四川省的页岩气开发,制订了在2020年前新增100亿立方米页岩气产能的计划。页岩气主要成分为CH4,请回答下列问题:
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO与H2的混合气),已知:CH4与H2O(g)通入聚焦太阳能反应器,会发生下列反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=+206 kJ·mol1 ①;又知CH4(g)+2O2(g)
CO(g)+3H2(g) ΔH=+206 kJ·mol1 ①;又知CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH=802 kJ·mol1②,则CO2与H2O(g)反应生成CO的热化学方程式为_____________。
CO2(g)+2H2O(g) ΔH=802 kJ·mol1②,则CO2与H2O(g)反应生成CO的热化学方程式为_____________。
(2)用合成气生产CH3OH的反应为:CO(g)+2H2(g)![]() CH3OH(g) ΔH。在10 L的恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的转化率随温度的变化及不同压强下CO的转化率变化如图所示,p2和200 ℃时n(H2)随时间变化结果如表所示。
CH3OH(g) ΔH。在10 L的恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的转化率随温度的变化及不同压强下CO的转化率变化如图所示,p2和200 ℃时n(H2)随时间变化结果如表所示。

p2和200 ℃时n(H2)随时间变化
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 5 | 4 | 4 |
①ΔH________0(填“<”“=”或“>”)。
②你认为可同时提高反应速率和H2转化率的措施是___________________(列举两条即可)。
③下列说法正确的是_________(填字母)。
A.温度越高,该反应的平衡常数越大
B.达平衡后再充入稀有气体,H2转化率将提高
C.体系内气体压强不变时,反应达到最大限度
D.图中压强p1<p2
④在p2和200 ℃时,反应0~3 min内,用CH3OH表示的平均反应速率v(CH3OH)=
___________________。
⑤在p2和200 ℃时,达平衡后再加入2 mol CO、2 mol H2、2 mol CH3OH,化学平衡______________(填“向正反应方向移动”“向逆反应方向移动”或“不移动”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g) ΔH=-a kJ·mol-1
2HI(g) ΔH=-a kJ·mol-1
已知:
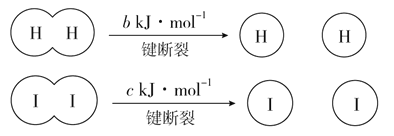
(a、b、c均大于零)
下列说法不正确的是
A. 反应物的总能量高于生成物的总能量
B. 断开1 mol H—H键和1 mol I—I键所需能量大于断开2 mol H—I键所需能量
C. 断开2 mol H—I键所需能量约为(c+b+a)kJ
D. 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com