
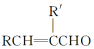 +H2O
+H2O ;E中含氧官能团的名称:羧基.
;E中含氧官能团的名称:羧基. +
+ $→_{加热}^{浓硫酸}$
$→_{加热}^{浓硫酸}$ +H2O.
+H2O.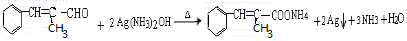 .
. .
.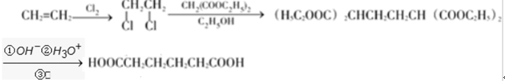 .
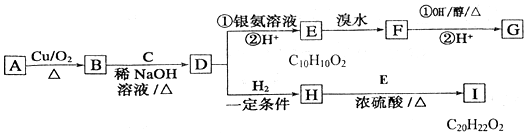
. 分析 I.物质A为生活中常见的有机物,只含有C、H、O三种元素,且它们的质量比为9:2:4,则N(C):N(H):N(O)=$\frac{9}{12}$:$\frac{2}{1}$:$\frac{4}{16}$=3:8:1,最简式为C3H8O,最简式中H原子已经饱和碳的四价结构,故分子式为C3H8O,其A能发生催化氧化反应生成B,则A为CH3CH2CH2OH,B为CH3CH2CHO,B与C发生信息中的反应生成D,D为烯醛,而D与银氨溶液发生氧化反应生成E,结构E的分子式可知,D分子式为C10H10O,由B、D分子式可知C的分子式为C10H10O+H2O-C3H6O=C7H6O,而物质D是一种芳香族化合物,故C为 ,D
,D ,E
,E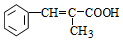 ,E与溴水发生加成反应生
,E与溴水发生加成反应生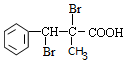 ,F发生消去反应生成G.D与氢气发生加成反应生成H
,F发生消去反应生成G.D与氢气发生加成反应生成H ,H与E发生酯化反应生
,H与E发生酯化反应生 ;
;
II.以乙烯、CH2(COOC2H5)2的乙醇溶液为有机反应原料制HOOCCH2CH2CH2CH2COOH,先乙烯加成生成二卤代烃,再发生R-Cl$→_{C_{2}H_{5}OH}^{CH_{2}(COOC_{2}H_{5})_{2}}$RCH(COOC2H5)2$\underset{\stackrel{①O{H}^{-}②{H}_{3}{O}^{+}}{→}}{③△}$RCH2COOH以此来解答.
解答 解:(1)A为CH3CH2CH2OH,名称为1-丙醇;C的结构简式为 ;E中含氧官能团的名称为羧基,
;E中含氧官能团的名称为羧基,
故答案为:1-丙醇; ;羧基;→
;羧基;→
(2)由上述分析可知,A→B为氧化反应; D→H为加成或还原反应,
故答案为:氧化反应;加成或还原反应;
(3)H到I的化学方程式 +
+ $→_{加热}^{浓硫酸}$
$→_{加热}^{浓硫酸}$ +H2O,
+H2O,
故答案为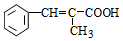 +
+ $→_{加热}^{浓硫酸}$
$→_{加热}^{浓硫酸}$ +H2O;
+H2O;
(4)D到E过程中的①的反应化学方程式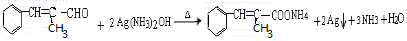 ,
,
故答案为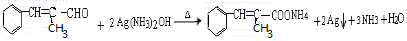 ;
;
(5) 中-COOH、-Br均与NaOH反应,1molF与足量的氢氧化钠水溶液反应最多消耗3mol NaOH,
中-COOH、-Br均与NaOH反应,1molF与足量的氢氧化钠水溶液反应最多消耗3mol NaOH,
故答案为:3;
(6)F的结构式为 ,F发生消去反应生成G,与溴原子所在碳原子相邻的碳有氢原子,才能发生消去反应,生成G的结构分别为
,F发生消去反应生成G,与溴原子所在碳原子相邻的碳有氢原子,才能发生消去反应,生成G的结构分别为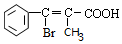 ,
,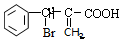 ,G的可能结构为2种,
,G的可能结构为2种,
故答案为:2;
(7)E的同分异构体符合i.该物质水解产物之一为乙酸,含-COOCH2CH3,
ii.苯环上的一氯代物只有两种结构,苯环上只有2种H,满足条件的结构简式为 ,
,
故答案为: ;
;
II.以乙烯、CH2(COOC2H5)2的乙醇溶液为有机反应原料制HOOCCH2CH2CH2CH2COOH,先乙烯加成生成二卤代烃,再发生R-Cl$→_{C_{2}H_{5}OH}^{CH_{2}(COOC_{2}H_{5})_{2}}$RCH(COOC2H5)2$\underset{\stackrel{①O{H}^{-}②{H}_{3}{O}^{+}}{→}}{③△}$RCH2COOH,则合成路线流程 ,
,
故答案为: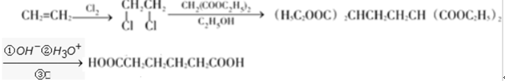 .
.
点评 本题考查有机物的合成,为高频考点,把握合成流程中官能团的变化、碳链变化、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度中等.


科目:高中化学 来源: 题型:解答题
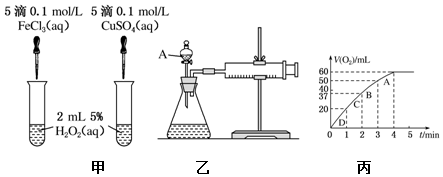
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.08g镁铝合金中含有镁和铝的质量分别为1.92g、2.16g | |
| B. | 生成沉淀的最大质量为10.88g | |
| C. | 若白色沉淀只有Mg(OH)2,该NaOH溶液的浓度至少为0.96mol/L | |
| D. | 溶解4.08 g镁铝合金时,剩余盐酸的物质的量为0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蒸馏烧瓶中盛约$\frac{1}{3}$体积的自来水,并放入几粒沸石[KS5UKS5U] | |
| B. | 可以不用温度计 | |
| C. | 冷水从冷凝管上口入,下口出 | |
| D. | 取少量收集到的液体滴入硝酸银和稀硝酸,无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B能形成离子化合物,且A离子半径小于B离子半径 | |
| B. | A、D能形成离子化合物DA5,与H2O反应能生成A的单质 | |
| C. | C、D的简单氢化物中只有D溶于水,其水溶液呈酸性 | |
| D. | E的两种氢化物中所有化学键种类完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
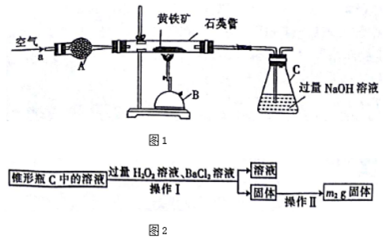
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 证明乙二酸具有还原性 | 向乙二酸溶液中滴加2 滴KMnO4溶液 |
| B | 制备Fe(OH)3胶体 | 将NaOH溶液滴加到饱和FeCl3溶液中 |
| C | 铝可以从铜盐溶液中置换铜 | 将久置在空气中的铝片放入CuSO4溶液中 |
| D | 检验蔗糖是否水解 | 取蔗糖溶液,加3~5滴稀硫酸,水浴加热5min,取少量溶液,加入银氨溶液加热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
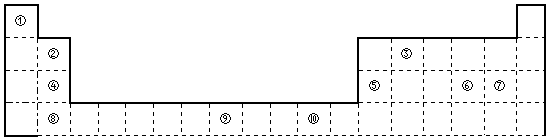
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com