
关于原电池和电解池的叙述正确的是( )
A.原电池中失去电子的电极为正极
B.原电池的负极、电解池的阳极都发生氧化反应
C.原电池的两极一定是由活动性不同的两种金属组成
D.电解时电解池的阴极一定是阴离子放电
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
| A. | Al2O3可用作耐火材料,用小苏打发酵面团制作馒头 | |
| B. | 碳素钢的熔点比纯铁低、司母戊鼎的主要成分是铜合金 | |
| C. | “海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化 | |
| D. | 绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省德州市高二上10月月考化学试卷(解析版) 题型:选择题
无水氯化铝是一种重要的催化剂,工业上由Al2O3制备无水氯化铝的反应为2Al2O3(s)+6Cl2(g)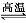 4AlCl3(g)+3O2(g) ΔH>0。下列分析错误的是( )
4AlCl3(g)+3O2(g) ΔH>0。下列分析错误的是( )
A.增大反应体系的压强,反应速率增大
B.加入碳粉,平衡向右移动,原因是碳与O2反应,降低了生成物的浓度且放出热量
C.电解熔融的Al2O3和AlCl3均能得到单质铝
D.升高温度,反应的平衡常数将增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省德州市高二上10月月考化学试卷(解析版) 题型:选择题
1mol白磷转化为红磷时放出18.39kJ热量,已知:P4(白磷,s)+5O2(g)=2P2O5(s) ΔH=-a kJ/mol(a>0);4P(红磷,s)+5O2(g)=2P2O5(s) ΔH=-bkJ/mol(b>0),则a和b的关系是( )
A.a > b B. a = b C.a < b D.无法确定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省徐州市高一上第一次月考化学卷(解析版) 题型:填空题
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①维生素C能增强人体对疾病的抵抗能力,促进人体生长发育,中学生每天要补充60mg的维生素C。下列物质含有丰富维生素C的是 (填字母)。
A.牛肉 B.辣椒 C.鸡蛋
②青少年及成人缺乏某种微量元素将导致甲状腺肿大,而且会造成智力损害,该微量元素是 ( 填字母)
A.碘 B.铁 C.钙
③蛋白质是人体必需的营养物质,它在人体内最终分解为 (填字母)。
A.葡萄糖 B.氨基酸 C. 脂肪酸
脂肪酸
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是 。
②玻璃是重要的硅酸盐产品。生产玻璃时,石灰石与石英反应的化学方程式为 。
③铁是人们生活中常用的金属材料,请列举两种防止铁制品被腐蚀的方法: , 。
(3)保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处。
①空气质量报告的各项指标可以反映出各地的空气质量。下列各项中目前未列入我国空气质量报告的是 (填字母 )。
)。
A.SO2
B.NO2
C.CO2
D.PM2.5
E.氯氟烃
②垃圾应分类收集。以下物质应放置于贴有“ ”标志垃圾筒的是 (填字母)。
”标志垃圾筒的是 (填字母)。
A.废电池 B.废铝制的易拉罐 C.建筑固弃物、渣土
③pH< 的雨水称为酸雨;向煤中加入适量的 ,可以大大减少燃物产物中SO2的量。
④天然水中杂质较多,常需加入明矾,ClO2等物质处理后才能饮用。加入ClO2的作用是  。
。
⑤对汽车加装尾气催化净化装置,可以使其中的NO、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省徐州市高一上第一次月考化学卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.11.2 L H2中含有氢原子的个数为NA
B.在标准状况下,22.4 L H2O中含有氢原子的个数为2NA
C.32 g O3中含有氧原子的个数为2NA
D.1 mol/L NaCl溶液中含有钠离子的个数为NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第一次月考化学试卷(解析版) 题型:填空题
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示, K值大小与温度的关系是:温度升高,K值 。(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g) +H2O(g)  CO2(g) +H2 (g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=mol·L-1·min-1。t℃时物质浓度(mol·L-1)的变化:
CO2(g) +H2 (g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=mol·L-1·min-1。t℃时物质浓度(mol·L-1)的变化:
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min~4min之间反应处于 状态;c 1数值 0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是 (单选),表中5min~6min之间数值发生变化,可能的原因是 (单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大铁的量可以使反应速率加快 | |
| B. | 将生成的气体在空气中冷却可获得钠 | |
| C. | 每生成1molH2,转移的电子数约为4×6.02×1023 | |
| D. | 该反应条件下铁的金属性比钠强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com