
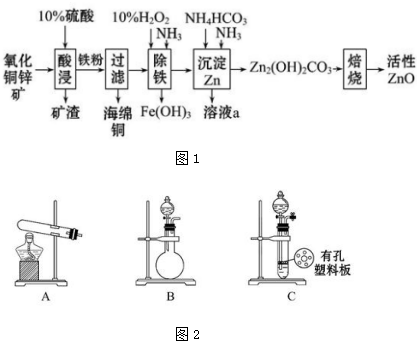
分析 氧化铜锌矿经废酸浸取后过滤,可得到硫酸铜、硫酸锌溶液;向酸浸液中加铁可还原出铜,经过滤可得铜和硫酸亚铁、硫酸锌的混合液;然后加入双氧水和氨气,将亚铁转化为氢氧化铁沉淀而除去;后向滤液中加氨气和碳酸氢铵等将锌离子转化为Zn2(OH)2CO3,最后焙烧,Zn2(OH)2CO3受热分解得到氧化锌.
(1)相同条件下,溶度积常数大的物质先溶解;
(2)①A装置为固体加热制备气体,实验室用氯化铵和氢氧化钙来制备氨气;
②装置B为液体与固体反应不需要加热的装置;
(3)由于NH4HCO3受热易分解同时也为了 减小碱式碳酸锌晶体的溶解度,氨解需降温冷却;
(4)从题给信息写出反应物和生成物,配平即可.
解答 解:(1)相同条件下,溶解度大的物质先溶解;因在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)<Ksp(ZnS),
故答案为:>;
(2)①A装置为固体加热制备气体,实验室用氯化铵和氢氧化钙来制备氨气,所以选A,
故答案为:A;
②装置B为液体与固体反应不需要加热的装置,则可以选用浓氨水、碱石灰来制备氨气;
故答案为:浓氨水、碱石灰;
(3)根据上面的分析可知,氨解反应需降温冷却的原因为NH4HCO3受热易分解同时也为了 减小碱式碳酸锌晶体的溶解度,
故答案为:防止氨水、碳酸氢铵分解,减小碱式碳酸锌的溶解度;
(5)由题给信息可知,反应物为2Fe(OH)3、ClO-、OH-,生成物之一为FeO42-,因铁在反应中化合价升高,故氯的化合价降低,故另一产物为Cl-,根据元素守恒,还有水是产物.根据化合价升降法配平此方程式为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O.
故答案为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O.
点评 本题属于工艺流程图方面题目.要搞清实验目的和题给信息,结合流程和题目设问正确解题.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
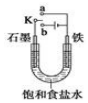 某课外活动小组同学用如图装置进行实验,试回答下列问题
某课外活动小组同学用如图装置进行实验,试回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑥ | B. | ②③④ | C. | ②④⑤ | D. | ③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com