
有一瓶因部分氧化而变质的亚硫酸钠试剂,测定它的纯度,通过下列操作:
①称取样品Wg
②溶解样品
③在溶液中加入过量的用盐酸酸化了的氯化钡溶液
④过滤和洗涤沉淀
⑤烘干并称量沉淀得m(g)
请回答下列问题:
(1)氯化钡溶液要用盐酸酸化的目的是______;
反应的离子方程式是________;
(2)氯化钡溶液过量的原因是______;
如何判断过量:________;
离子方程式是_______;
(3)判断沉淀是否洗净的方法是________;
(4)计算亚硫酸钠的纯度为________;
(5)写出亚硫酸钠样品变质的有关化学方程式是_______.
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:走向清华北大同步导读·高一化学 题型:058
有一Na2SO3晶体,因部分氧化而变质,为了测定样品中杂质的质量分数,根据下图的实验步骤进行测定,按要求填写下列空白:
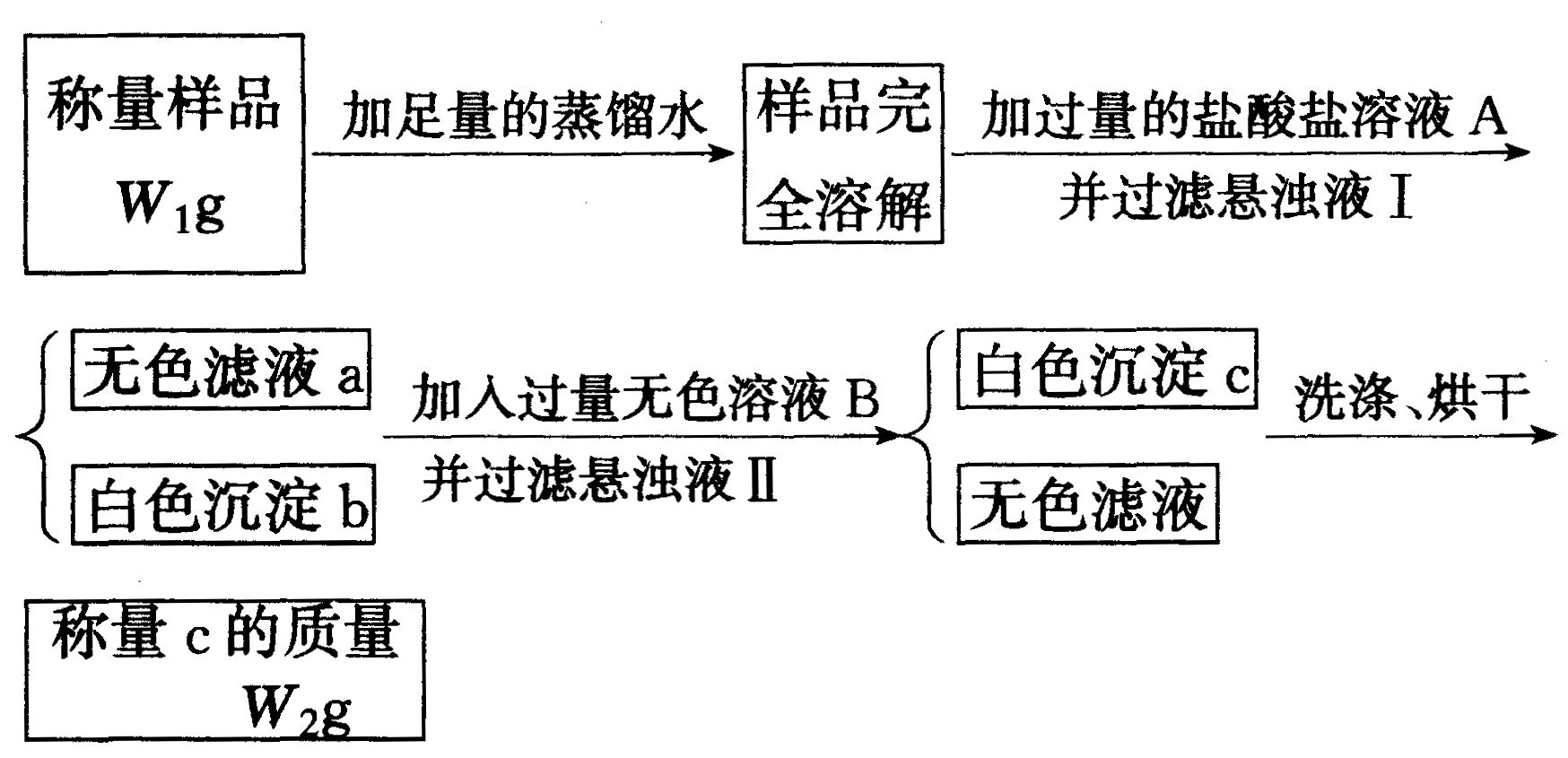
(1)在托盘天平上称量样品时,应先在天平的两盘中各放一张________.
(2)A的化学式为________,A必须过量的原因是________.
(3)确定A是否过量的方法是:①静置悬浊液Ⅰ,然后在上层澄清液中继续滴入几滴________溶液,若________,则证明A已过量;②在滤液a中滴加________溶液,若无白色沉淀生成,则证明A不足,则还需要继续在滤液a中加入A并过滤.
(4)白色沉淀b含有________;无色溶液B通常是________.
(5)通过以上测定可得样品中杂质的质量分数的计算关系式为________.
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058

(1)溶解样品所用的仪器是________。
(2)向样品溶液中加入的A溶液是________;
A要酸化的目的是________;不用硝酸酸化的原因是________;A要过量的原因是________。
(3)通过检验无色溶液a来判断A是否过量。取少许a溶液,滴加________,若则表明A已过量。
(4)白色沉淀b在烘干前,应在过滤器中用蒸馏水多次洗涤,其原因是________;为了检验沉淀是否洗净,应在最后几滴洗出液中滴加________,若________则表明沉淀已洗净。
(5)通过以上实验测定,其样品纯度的数学表达式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:058
有一纯净的亚硫酸钠试剂,因部分氧化而变质,为了测定试剂的纯度,根据下图所给出的方案进行实验,请按要求填写以下各项空白。

(1)溶解样品所用的仪器是________。
(2)向样品溶液中加入的A溶液是________;
A要酸化的目的是________;不用硝酸酸化的原因是________;A要过量的原因是________。
(3)通过检验无色溶液a来判断A是否过量。取少许a溶液,滴加________,若则表明A已过量。
(4)白色沉淀b在烘干前,应在过滤器中用蒸馏水多次洗涤,其原因是________;为了检验沉淀是否洗净,应在最后几滴洗出液中滴加________,若________则表明沉淀已洗净。
(5)通过以上实验测定,其样品纯度的数学表达式为________。
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第19~26期 总第175~182期 人教课标版 题型:022
实验室有一瓶因密闭不好而变质的固体烧碱.已知该药品含有
92%的NaOH、1%的Na2CO3、5%的Na2CO3·10H2O、2%的H2O.某同学取该样品a g溶于水后加入含2.92 g HCl的盐酸40 mL,充分反应后,再用一定量的氢氧化钠溶液中和剩余的盐酸至恰好完全反应,将反应后的溶液蒸干并将固体干燥.若计算蒸干后固体的质量,题目给出的数据是否充足?
________(填“是”或“否”).如果数据充足,求算的依据是________,固体的质量为________.(写出计算过程.如果数据不充足,后两问不需要回答)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com