
分析 (1)NaHSO4是强酸强碱酸式盐,完全电离出Na+、H+、SO42-离子;
(2)氢硫酸为二元弱酸,分步电离;
(3)碳酸钠是强碱弱酸盐,碳酸根离子为多元弱酸的酸根离子,分步水解,以第一步为主,用可逆号;
(4)氯化铁是强酸弱碱盐,溶液中铁离子水解,溶液显酸性;
解答 解:(1)NaHSO4是强酸强碱酸式盐,属强电解质,完全电离用“═”,电离出Na+、H+、SO42-离子,其电离方程式为:NaHSO4=Na++H++SO42-,
故答案为:NaHSO4=Na++H++SO42-;
(2)氢硫酸为二元弱酸,H2S的水溶液中存在平衡:H2S?HS-+H+ 和HS-?S2-+H+,故答案为:H2S?H++HS-、HS-?H++S2-;
(3)碳酸根离子分步水解的离子方程式:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?CO32-+OH-,故答案为:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?CO32-+OH-;
(4)氯化铁是强酸弱碱盐,溶液中铁离子水解,溶液显酸性,离子方程式为:Fe3++3H2O?Fe(OH)3+3H+,
故答案为:Fe3++3H2O?Fe(OH)3+3H+;
点评 本题考查了电离方程式、水解离子方程式的书写,注意多元弱酸分步电离,多元弱酸阴离子分步水解,掌握书写方法并能灵活运用是正确解答此类题的关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “纳米碳”属于“纳米材料”,若将纳米碳均匀地分散到蒸馏水中,所形成的物质能透过滤纸,不能透过半透膜,静置后会析出黑色沉淀 | |
| B. | 维生素C又称“抗坏血酸”,在人体内有重要的功能,是因为维生素C具有氧化性 | |
| C. | 表面打磨过的铝箔,在空气中加热至熔化也不滴落是因为表面生成了熔点很高的氧化铝薄膜包裹在铝的外面 | |
| D. | 氨很容易液化,液化时放热,液化后得到氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是实验室制取氨气的装置图,请回答:
如图是实验室制取氨气的装置图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
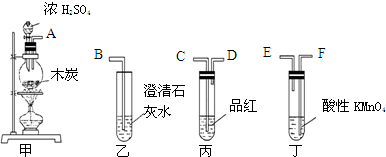
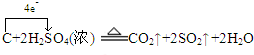 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液保存在具有橡皮塞的玻璃试剂瓶中 | |
| B. | 少量的钠保存在煤油中 | |
| C. | 氢氟酸盛装在细口玻璃瓶中 | |
| D. | 新制的氯水通常保存在棕色玻璃试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3和NaHCO3均可与HCl反应 | |
| B. | Na2CO3能与石灰水反应而NaHCO3不能 | |
| C. | Na2CO3的热稳定性比NaHCO3的强 | |
| D. | Na2CO3比NaHCO3易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| B. | 2L 0.5mol/L亚硫酸溶液中含有的H+两种数为2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 咖啡加糖 | B. | 炒菜加味精 | ||
| C. | 酱油加铁强化剂 | D. | 加工食品加防腐剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com