
| A、Na2HPO4溶于水:Na2HPO4=2Na++H++PO43- |
| B、NaHSO4熔化:NaHSO4=Na++H++SO42- |
| C、HF溶于少量水中:HF=H++F- |
| D、(NH4)2SO4溶于水:(NH4)2SO4=2NH4++SO42- |


科目:高中化学 来源: 题型:
| A、常温常压下,6g二氧化硅含有Si-O键数目为2NA |
| B、54克Al与氢氧化钠反应产生气体67.2L |
| C、Na与足量O2反应生成1mol Na2O或1mol Na2O2均失去2NA电子 |
| D、各5.6g铁分别与足量的盐酸反应,电子转移总数均为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al与S直接化合可以得到Al2S3,Fe与S直接化合也可以得到Fe2S3 |
| B、水银、水玻璃、胆矾都是纯净物 |
| C、HCl、NH3、BaSO4都是电解质 |
| D、丁达尔现象可以用来区别胶体和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、产物B的状态只能为固态或液态 |
| B、平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1 |
| C、保持体积不变,向平衡体系中加入B,平衡不可能向逆反应方向移动 |
| D、若开始时向容器中加入1mol B和1mol C,达到平衡时放出热量QkJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2都是还原产物 |
| B、H2都是氧化产物 |
| C、CaH2中的氢元素既被氧化又被还原 |
| D、氧化产物与还原产物的质量比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下11.2L CCl4和11.2L CO2分子数相同 |
| B、CH4的摩尔质量为16g |
| C、3.01×1023个SO2分子的质量为32g |
| D、标准状况下,1mol任何物质体积均为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠也可以保存在CCl4中 |
| B、钠着火时可以砂土来扑灭 |
| C、除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| D、除去Al粉中混有的Mg:加足量NaOH溶液后,过滤、洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
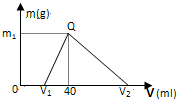 (1)15.6g Na2X含Na+0.4moL,则Na2X的摩尔质量为
(1)15.6g Na2X含Na+0.4moL,则Na2X的摩尔质量为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com