
| A. | NO | B. | NO2 | C. | N2O | D. | N2O3 |
分析 10HNO3(稀)+4Zn=4Zn(NO3)2+a+5H2O,依据原子个数守恒,a中物质含有2个N,1个O,反应中硝酸中的+5价N化合价降低,Zn化合价由0价升高到+2价,依据氧化还原反应得失电子守恒、原子个数守恒判断a,据此解答.
解答 解:依据原子个数守恒,a中物质含有2个N,1个O,10HNO3(稀)+4Zn=4Zn(NO3)2+a+5H2O,反应中硝酸中的+5价N化合价降低,Zn化合价由0价升高到+2价,4molZn共失去8mol电子,要使得失电子守恒,则硝酸2个+5价N 共得到8个电子,所以1个N得到4个电子,化合价从+5价降为+1价,所以a为N2O,
故选C.
点评 本题考查了氧化还原反应,侧重考查氧化还原方程式书写,明确得失电子守恒、原子个数守恒规律即可解答,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温常压下,0.1NA个HCl分子的体积为22.4L | |
| B. | 标准状况下,22.4L氖气含有2NA个原子 | |
| C. | 1L 0.2mol/L硫酸铁溶液中含有的SO42-离子数目为0.6NA | |
| D. | 1mol氖气中含有的电子数目为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol OH-含有的电子数为9NA | |
| B. | 常温常压下,NO2和N2O4的混合物23g中含有NA个氧原子 | |
| C. | 标准状况下,2.8gN2和2.24L CO所含电子数均为1.4NA | |
| D. | 标准状况下,22.4 L 乙醇中含有NA个乙醇分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
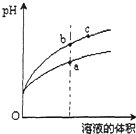 某温度下,相同pH的盐酸和醋酸分别加水稀释,pH随溶液体积变化的曲线如图所示,据图判断下列说法正确的是( )
某温度下,相同pH的盐酸和醋酸分别加水稀释,pH随溶液体积变化的曲线如图所示,据图判断下列说法正确的是( )| A. | b点酸的总浓度大于a点酸的总浓度 | |
| B. | c点溶液的导电性比b点强 | |
| C. | a点Kw的数值比c点溶液的Kw的数值大 | |
| D. | b点水电离产生的c(H+)比a点大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | 离子浓度(mol•L-1) | |
| 还原前 | 还原后 | |
| SO42- | 3.20 | 3.50 |
| Fe2+ | 0.15 | 3.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将20 g NaOH 溶解在500mL 水中 | |
| B. | 将22.4 L HCl 气体溶于水配成1 L 溶液 | |
| C. | 将1 L 10 mol•L-1浓盐酸加入9 L 水中 | |
| D. | 将10 g NaOH 溶解在少量水中,恢复至室温,再加蒸馏水直到溶液体积为250 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com