
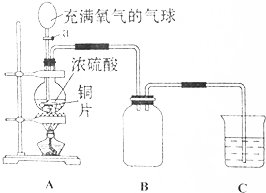
 小明同学设计了如图所示装置探究铜跟浓硫酸的反应.先关闭活塞a,加热至烧瓶中不再有气泡产生时,反应停止,此时烧瓶中铜片仍有剩余.接着再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢减少.
小明同学设计了如图所示装置探究铜跟浓硫酸的反应.先关闭活塞a,加热至烧瓶中不再有气泡产生时,反应停止,此时烧瓶中铜片仍有剩余.接着再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢减少.分析 (1)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水;
(2)二氧化硫密度大于空气密度,应采用向上排气法,导气管应长进短出;
(3)二氧化硫表现还原性,则反应中硫元素化合价升高,例如二氧化硫与氧气反应生成三氧化硫;
(4)二氧化硫有毒,应进行尾气处理,二氧化硫为酸性氧化物,能够与氢氧化钠溶液反应,用氢氧化钠溶液吸收二氧化硫.
解答 解:(1)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,化学方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)二氧化硫密度大于空气密度,应采用向上排气法,导气管应长进短出,故B处错误;
故选:B;
(3)二氧化硫与氧气反应生成三氧化硫,方程式:2SO2+O2?$\frac{\underline{\;催化剂\;}}{△}$2SO3,反应中二氧化硫表现还原性;
故答案为:2SO2+O2?$\frac{\underline{\;催化剂\;}}{△}$2SO3;
(4)二氧化硫有毒,应进行尾气处理,二氧化硫为酸性氧化物,能够与氢氧化钠溶液反应,用氢氧化钠溶液吸收二氧化硫,氢氧化钠化学式为:NaOH;
故答案为:NaOH.
点评 本题考查了元素化合物知识,侧重考查浓硫酸的性质,熟悉浓硫酸的强的氧化性是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
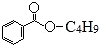 ,下列说法错误的是( )
,下列说法错误的是( )| A. | X难溶于水 | B. | X的分子式为C11H14O2 | ||
| C. | 组成为-C4H9的烃基有3种 | D. | X能发生加成反应、取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、纯碱、漂白粉 | B. | 硫酸、烧碱、小苏打 | ||
| C. | 硫酸氢钠、生石灰、醋酸钠 | D. | 磷酸、熟石灰、苛性钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32g氧气与足量锂完全反应得到的电子数为2NA | |
| B. | 在1L2mol•L-1MgCl2溶液中含有的Cl-数为2NA | |
| C. | 标准状态下,2.24LCO2与2.24LH2O中所含原子数均为0.3NA | |
| D. | 标准状况下,11.2L氯气与足量NaOH溶液反应转移的电子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表:
T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表:| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有一个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ•mol,I2=1817kJ•mol-1,I3=2745kJ•mol-1,I4=11575kJ•mol-1 |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
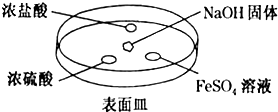
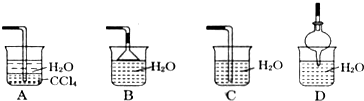

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
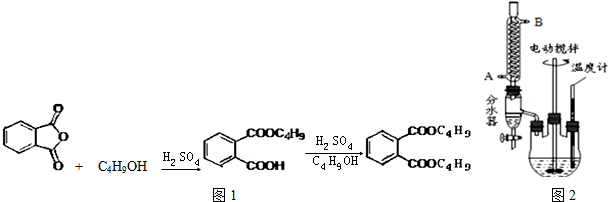
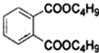 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$ +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
在 10—9m~10—7m范围内,对原子、分子进行操纵的纳米超分子技术往往能实现意想不到的变化。纳米铜粒一遇到空气就会剧烈燃烧,甚至发生爆炸。下列说法正确的是
10—9m~10—7m范围内,对原子、分子进行操纵的纳米超分子技术往往能实现意想不到的变化。纳米铜粒一遇到空气就会剧烈燃烧,甚至发生爆炸。下列说法正确的是
A.纳米铜是一种新型化合物 B.纳米铜颗粒比普通铜更易与氧气发生反应
C.纳米铜与普通铜所含铜原子的种类不同 D.纳米铜无需密封保存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com