
【题目】氮氧化物和硫氧化物是常见的空气污染物,含氮氧化物和硫氧化物的尾气需处理后才能排放。
Ⅰ.氮氧化物的处理
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为_________。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为NO+NO2+2OH=2NO2-+H2O,2NO2+2OH= NO2-+NO3-+H2O,吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是_________(填化学式)。
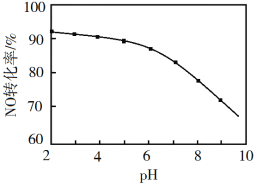
(3)NO的氧化吸收。在酸性NaClO溶液中,HClO氧化NO生成Cl和NO3-。其他条件相同,NO转化为NO3-的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是_________。
Ⅱ.煤燃烧排放的烟气中SO2和NOx的处理
采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有SO2和NOx的烟气,反应温度为323K,NaClO2溶液浓度为5×103mol·L1 。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
(4)写出NaClO2溶液脱硫过程中主要反应的离子方程式________。增加压强,NO的转化率_________(填“提高”“不变”或“降低”)。
(5)由实验结果可知,脱硫反应速率大于脱硝反应速率。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是_________。
【答案】2NH3+2O2![]() N2O+3H2O NaNO3 溶液pH越小,溶液中HClO的浓度越大,氧化NO的能力越强 2SO2+ClO2-+4OH-=2SO42-+2H2O+Cl- 提高 NO溶解度较低或脱硝反应活化能较高
N2O+3H2O NaNO3 溶液pH越小,溶液中HClO的浓度越大,氧化NO的能力越强 2SO2+ClO2-+4OH-=2SO42-+2H2O+Cl- 提高 NO溶解度较低或脱硝反应活化能较高
【解析】
(1)NH3与O2在加热和催化剂作用下生成N2O,同时生成水;
(2)反应生成NaNO2和NaNO3;
(3)NaClO溶液的初始pH越小,HClO的浓度越大,氧化能力强;
(4)亚氯酸钠具有氧化性,则NaClO2溶液脱硫过程中将SO2氧化为SO42-,ClO2-被还原为Cl-,结合电子守恒、电荷守恒及原子守恒书写方程式;正反应是体积减小的反应,则增加压强,NO的转化率提高;
(5)由实验结果可知,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是二氧化硫的还原性强,易被氧化,还可能是NO溶解度较低或脱硝反应活化能较高。
(1)NH3与O2在加热和催化剂作用下发生氧化还原反应生成N2O和水,反应的化学方程式为2NH3+2O2![]() N2O+3H2O;
N2O+3H2O;
(2)根据气体的成分及发生的反应可知,反应生成NaNO2和NaNO3,所以吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是NaNO3;
(3)NaClO溶液的初始pH越小,则NaClO与溶液中的H+结合形成的HClO的浓度就越大,HClO的浓度越大,其氧化能力强,因此可提高NO转化率;
(4)亚氯酸钠具有氧化性,则NaClO2溶液脱硫过程中将SO2氧化为SO42-,ClO2-被还原为Cl-,结合电子守恒、电荷守恒及原子守恒书写方程式为:2SO2+ClO2-+4OH-=2SO42-+2H2O+Cl-;脱硝反应的正反应是气体体积减小的反应,根据平衡移动原理:增加压强,平衡正向移动,所以NO的转化率提高;
(5)由实验结果可知,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是二氧化硫的还原性强,易被氧化,还可能是NO溶解度较低或脱硝反应活化能较高。


科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W在周期表中的相对位置如图,四种元素的原子最外层电子数之和为20。下列说法正确的是
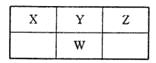
A.W位于第三周期ⅥA族
B.元素最高正价:Z>Y>X
C.简单气态氢化物稳定性:W>Y>X
D.工业上催化氧化Y的氢化物可用于制备其含氧酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物,只可能含有C、H、O三种元素,在标况下,其蒸气的密度是H2的21倍。测得其质量为10.5g,在氧气中充分燃烧,生成33g二氧化碳和13.5g水,求该化合物的分子式,并写出其所有可能结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,改变饱和氯水的pH,得到部分含氯微粒的物质的量分数与pH的关系如图所示。下列叙述不正确的是
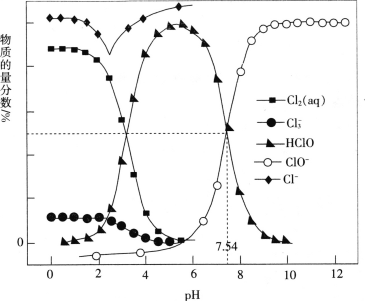
A.pH=1的氯水中,c(Cl2)>c(Cl3-)>c(HClO)>c(ClO-)
B.氯水中的Cl2、ClO-、HClO均能与K2S发生反应
C.已知常温下反应Cl2(aq)+Cl-(aq)![]() Cl3- (aq)的K=0.191,当pH增大时,K减小
Cl3- (aq)的K=0.191,当pH增大时,K减小
D.该温度下,HClO![]() H++ClO-的电离常数Ka=10-7.54
H++ClO-的电离常数Ka=10-7.54
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合元素周期表回答下列问题:
(1)①表中实线是元素周期表的部分边界,请在图1中用实线补全元素周期表的边界________
②请画出金属与非金属的分界线________
③请在方框中(图3)按氦元素的式样写出h元素原子的相关信息________
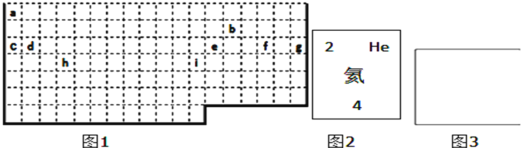
(2)X、Y、Z是周期表中相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31。
①X是______, Z是______(填写元素名称)
②X, Y, Z 三种元素的简单离子半径大小顺序是_____________________________
③三种元素形成的单质氧化性最强的化学式为______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图1所示。下列说法正确的是
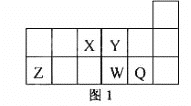
A. 元素X与元素Z的最高正化合价之和的数值等于8
B. 原子半径的大小顺序为:rX>rY>:rZ>rW>rQ
C. 离子Y2-和Z 3+的核外电子数和电子层数都不相同
D. 元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是![]()
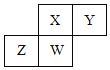
A.最简单气态氢化物的热稳定性:![]() X
X![]() W
W![]() Z
Z
B.最高价氧化物对应的水化物的酸性:![]() W
W![]() Z
Z
C.原子半径:![]() Z
Z![]() Y
Y![]() X
X
D.元素X、Z、W的最高正价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示![]() 部分反应条件、产物省略
部分反应条件、产物省略![]() :
:
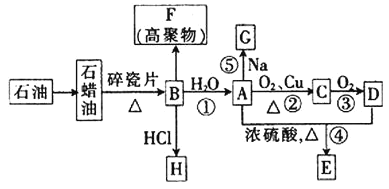
回答下列问题:
![]() 工业上,由石油获得石蜡油的方法称为_________,由石蜡油获得B的方法称为__________。
工业上,由石油获得石蜡油的方法称为_________,由石蜡油获得B的方法称为__________。
![]() ①决定化合物A的化学特性的原子团的名称为______________。
①决定化合物A的化学特性的原子团的名称为______________。
②![]() 到A的反应类型为_______,A到E的反应类型为____________。
到A的反应类型为_______,A到E的反应类型为____________。
③![]() 的分子式为_________;F的结构简式为___________。
的分子式为_________;F的结构简式为___________。
![]() 写出下列反应的化学方程式。
写出下列反应的化学方程式。
反应①:___________________________________________________;
反应②:___________________________________________________;
反应⑤:___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,B与D形成的化合物BD与C的单质C2电子总数相等,CA3分子结构为三角锥形,D与E可形成E2D与E2D2两种离子化合物,D与F是同族元素。根据以上信息,回答下列有关问题:
(1)写出基态时D的电子排布图________。
(2)写出化合物E2F2的电子式________,化合物ABC的结构式________。
(3)根据题目要求完成以下填空:
①BF32﹣中心原子杂化方式________;CA3中心原子杂化方式________;
②FD42﹣微粒中的键角________; FD3分子的立体构型________。
(4)F元素两种氧化物对应的水化物酸性由强到弱为__________,原因__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com