
【题目】(多选)氧化铜矿用稀硫酸溶解后所得酸浸液(含Cu2+、H+、SO42﹣、Mg2+、A13+、Fe2+) 经下列流程可制得高纯度硫酸铜晶体如图1: 
已知:该实验条件下,各金属离子沉淀的pH如图2所示.下列判断正确的是( )
A.沉淀1的主要成分为Al(OH)3和Fe(OH)3
B.溶液2中所含金属阳离子只有Mg2+
C.将溶液3蒸干即得CuSO45H2O晶体
D.若不加入NaClO溶液,对制得硫酸铜晶体的纯度将无影响
【答案】AD
【解析】解:氧化铜矿用稀硫酸溶解后所得酸浸液(含Cu2+、H+、SO42﹣、Mg2+、A13+、Fe2+),加NaClO溶液,把亚铁离子氧化为Fe3+ , 调节溶液的pH=4.7,由各金属离子沉淀的pH图可知,A13+、Fe3+转化为Al(OH)3和Fe(OH)3沉淀,过滤,沉淀1为Al(OH)3和Fe(OH)3 , 溶液1含有Cu2+、H+、SO42﹣、Mg2+ , 然后加NaOH,调节pH=6.7,Cu2+转化为Cu(OH)2沉淀,过滤,沉淀2为Cu(OH)2 , 溶液2主要含有Mg2+ , Cu(OH)2加硫酸生成溶液3为硫酸铜溶液,然后加热浓缩、冷却结晶得到硫酸铜晶体;A.由流程分析可知,沉淀1的主要成分为Al(OH)3和Fe(OH)3 , 故A正确;
B.溶液2主要含有Mg2+ , 还有少量的Cu2+、A13+、Fe3+ , 因为Cu2+、A13+、Fe3+不能全部转化为沉淀,故B错误;
C.从溶液中提取溶质时,加热浓缩、冷却结晶,不能加热干,故C错误;
D.若不加入NaClO溶液,在调节pH=4.7时,Fe2+不能转化为沉淀,在调节pH=6.7,Cu2+转化为Cu(OH)2沉淀,而此时Fe2+不能转化为沉淀,所以对制得硫酸铜晶体的纯度将无影响,故D正确.
故选AD.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】室温下,0.1mol/L的H2A溶液体系中,含A粒子的分布系数(平衡时某粒子的浓度占各粒子浓度之和的分数)与溶液 pH的关系如图所示.下列说法不正确的是( ) 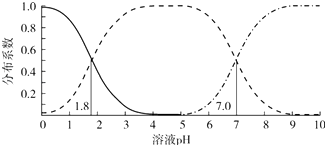
A.室温下,HA﹣的电离常数Ka2=1.0×10﹣7
B.室温下,0.1mol/L的NaHA溶液显酸性
C.室温下,0.2mol/L的H2A与0.1mol/L的NaOH溶液等体积混合,溶液pH=1.8
D.0.1mol/L的Na2A溶液中c(OH﹣)=c(H+)+c(HA﹣)+2c(H2A)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组比较中不正确的是( )
A. 稳定性:NH3>H2O
B. 碱性:NaOH>Mg(OH)2
C. 氧化性:F2>O2
D. 酸性: HClO4>H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素性质递变错误的是
A.Li、Be、B原子最外层电子数逐渐增多B.N、O、F氢化物的稳定性依次减弱
C.P、S、Cl最高正价依次升高D.Li、Na、K的金属性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 离子化合物一定不含共价键
B. 共价化合物中一定不含有离子键
C. 气态单质的分子中一定存在共价键
D. 非金属元素的化合物中一定不含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列溶液中,各组离子一定能够大量共存的是( )
A.使酚酞试液变红的溶液:Na+、Cl﹣、SO ![]() 、Fe3+
、Fe3+
B.常温下 ![]() =0.1mol?L﹣1的溶液:K+、Na+、SiO
=0.1mol?L﹣1的溶液:K+、Na+、SiO ![]() 、NO
、NO ![]()
C.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、MnO ![]() 、Cl﹣
、Cl﹣
D.澄清透明溶液:Al3+、Na+、SO ![]() 、HCO3﹣
、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数,下面叙述正确的是( )
A.标准状况下,11.2L CCl4所含分子数为0.5NA
B.1L 1mol/L的氯化钠溶液中,所含离子数为NA
C.常温下,4.4g CO2和N2O(不反应)混合物中所含有的原子数为0.3NA
D.1mol Cl2与足量的铁发生反应,转移的电子总数为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com