
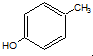
 �Լ���������ˮ��Ӧ
�Լ���������ˮ��Ӧ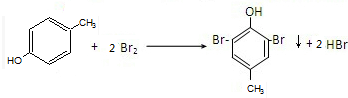
 ���Ѷ�ϩ������1��4�ӳ�
���Ѷ�ϩ������1��4�ӳ� +Cl2$\stackrel{����}{��}$
+Cl2$\stackrel{����}{��}$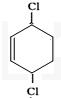
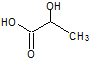 ����������������Ԫ��״�л���CH3CH��OH��COOH$��_{��}^{Ũ����}$
����������������Ԫ��״�л���CH3CH��OH��COOH$��_{��}^{Ũ����}$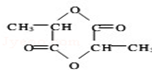 +2H2O
+2H2O ��
�� ���� ��1��ʵ�����Ʊ���Ȳ����̼������ˮ��Ӧ������Ȳ���������ƣ�
��2������ˮ������ղ����������ǣ�
��3���Լ�������Ũ��ˮ��Ӧ���DZ��ӷ������ǻ��Ա���Ӱ�죬��λ��ԭ�ӻ��ã�����ȡ����Ӧ��
��4�����Ѷ�ϩ������1��4�ӳɣ�����3��6-���Ȼ���ϩ��
��5����������к����ǻ����Ȼ����ܹ�������������ˮ���� ��
��
��6���ױ���Ũ���������¿���Ũ���ᷢ��ȡ����Ӧ����TNT��
��� �⣺��1��ʵ�����Ʊ���Ȳ������̼������ˮ��Ӧ������Ȳ���������ƣ���ӦΪCaC2+2H2O��Ca��OH��2+CH��CH����
�ʴ�Ϊ��CaC2+2H2O��Ca��OH��2+CH��CH����
��2�����������Ի�����ˮ������ղ����������ǣ���ѧ����ʽΪ����C6H10O5��n+nH2O$\stackrel{����}{��}$n C6H12O6��
�ʴ�Ϊ����C6H10O5��n+nH2O$\stackrel{����}{��}$n C6H12O6��
��3���Լ�������Ũ��ˮ��Ӧ���DZ��ӷ������ǻ��Ա���Ӱ�죬��λ��ԭ�ӻ��ã�����ȡ������Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��4�� ���Ѷ�ϩ������1��4�ӳɣ�����3��6-���Ȼ���ϩ����Ӧ����ʽΪ��
���Ѷ�ϩ������1��4�ӳɣ�����3��6-���Ȼ���ϩ����Ӧ����ʽΪ�� +Cl2$\stackrel{����}{��}$
+Cl2$\stackrel{����}{��}$ ��
��
�ʴ�Ϊ�� +Cl2$\stackrel{����}{��}$
+Cl2$\stackrel{����}{��}$ ��
��
��5������[CH3CH��OH��COOH]�����ǻ����Ȼ����ֹ����ţ����������ܹ���Ũ����������������Ԫ��״�������Ӧ�Ļ�ѧ��Ӧ����ʽΪ��CH3CH��OH��COOH$��_{��}^{Ũ����}$ +2H2O��
+2H2O��
�ʴ�Ϊ��CH3CH��OH��COOH$��_{��}^{Ũ����}$ +2H2O��
+2H2O��
��6���ױ���Ũ���������¿���Ũ���ᷴӦ����TNT����Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼�����л���Ӧ����ʽ����д����Ŀ�Ѷ��еȣ�ע�����ճ����л���Ӧ����ʽ����д��������ȷ��Ӧԭ��Ϊ�����Ĺؼ�������������ѧ�����Ӧ����ѧ֪ʶ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2s������Ժ�3p����γ�sp2�ӻ���� | |
| B�� | ϩ���е�̼̼˫����l���Ҽ���l���м���� | |
| C�� | �ɼ��Լ���ɵķ��ӣ�һ���Ǽ��Է��� | |
| D�� | ������sp3�ӻ�����Ĺ�����ƽ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | �� | |
| 4 | �� | ⑪ | ⑫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������c��d | B�� | �⻯����ȶ��ԣ�H2Y��HZ | ||
| C�� | ���ӵ������ԣ�X+��W3+ | D�� | ԭ�Ӱ뾶��X��W |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
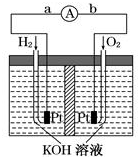 ����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã�ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش�
����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã�ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��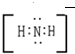 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ���̵����ӷ���ʽ��2Cu2++3SO32-��Cu2O��+SO42-+2SO2�� | |
| B�� | ��Ӧ���̵����ӷ���ʽ��2Cu2++3SO32-+2H2O��Cu2O��+SO42-+4H+ | |
| C�� | �������Na2SO3�����ڿ�����Һ��pH | |
| D�� | �����������£�����14.4g Cu2O���ʣ�ת�Ƶ���0.02mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com