
[化学——选修5:有机化学基础](15分)
某香料W的结构简式如图所示。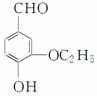
请按要求回答下列问题:
(1)有机物W中含氧不饱和官能团的名称为________。
(2)与有机物W互为同分异构体,能与NaHCO3溶液反应,且苯环上只有一个取代基的有_________________________________________________种(不含R—O—R′及R—O—COOH结构,R、R′代表烃基)。
(3)化合物Ⅱ是上述(2)同分异构体中的一种,可发生如下转化:
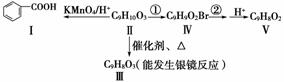
已知:与苯环直接相连的碳原子上有氢时,此碳原子才可被酸性KMnO4溶液氧化为羧基。
①写出化合物Ⅱ中含氧官能团的结构简式:________;
②由化合物Ⅱ也可直接生成化合物Ⅴ,设计反应①和②的目的是__________________________________________________________________。
③写出下列反应的化学方程式:
ⅰ.Ⅱ→Ⅲ:___________________________________________________;
ⅱ.化合物Ⅳ与NaOH水溶液共热:_______________________________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。
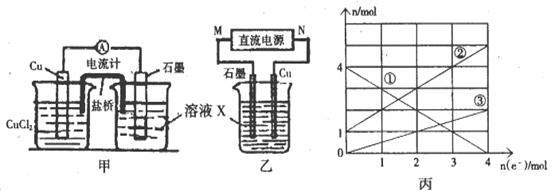
(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:
①图中X溶液是 ;
②原电池工作时,盐桥中的 离子(填“K+”或“Cl—”)不断进入X溶液中。
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是 极;
②图丙中的②线是____________离子的变化。
③当电子转移为2mol时,向乙烧杯中加入 L 5mol·L-1NaOH溶液才能使所有的金属阳离子沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。从环境保护的角度看,制备Na2FeO4较好的方法为电解法,其装置如图Ⅰ所示。
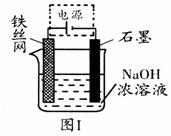
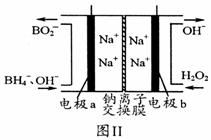
①电解过程中阳极的电极反应式为 。
②图Ⅰ装置中的电源采用 NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,电源工作原理如图Ⅱ所示。工作过程中该电源的正极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的数值,下列判断正确的是( )
A.常温常压下,22.4 L CH4中含有的C—H键数为4NA
B.4.6 g由NO2和N2O4组成的混合气体中含有的氧原子数为0.3NA
C.含0.2 mol H2SO4的浓硫酸与足量Cu反应,生成SO2的分子数为0.1NA
D.1 mol Na在足量O2中燃烧生成Na2O2,钠失去的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
(13分)下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。
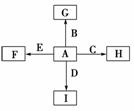
已知:
①单质中只有A为金属,在大气层高空释放的蒸气呈现明亮的橙黄色云雾,科学家由此可确定火箭在空中的位置;B、C、D为气体,E为固体;C、E为有色物质。
②B与D可以生成化合物J,A与J反应生成D和另一种化合物K,C与K反应的产物含漂白液的有效成分,F、G、I的水溶液呈碱性。
回答问题:
(1)化合物K的电子式为________。
(2)F的水溶液呈碱性的原因(用离子方程式表示)_____________________
______________________________________________________________,
写出I与J反应的化学反应方程式_________________________________
______________________________________________________________。
(3)实验室制备C的离子反应方程式为_____________________________。
(4)D在C中燃烧观察到的现象是_________________________________。
(5)可利用B与D生成化合物J的反应制成燃料电池,若1 g D在B中燃烧生成气态J时,放出120.9 kJ的热量,已知1 mol J 在汽化时吸热44.0 kJ,写出表示D的燃烧热的热化学方程式_______________________________________
_______________________________________________________________,
利用K作电解质溶液,写出该燃料电池的负极的电极反应方程式_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
2008年北京奥运会的国家游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成聚全氟乙丙烯。下列说法错误的是 ( )
A. 合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应
B. ETFE分子中可能存在“—CH2—CH2—CF2—CF2—”的连接方式
C.聚全氟乙丙烯分子的结构简式可能为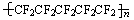
D.四氟乙烯分子中含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z和R分别代表4种元素,如果aXm+、bYn+、cZn-、dRm-四种离子的电子层结构相同,则下列关系正确的是 ( )
A.a-c=m-n B.a-b=n-m C.c-d=m+n D.b-d=m+n
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,生成物总能量高于反应物总能量的是
A.乙醇燃烧 B.氧化钙溶于水
C.锌粉和稀硫酸反应 D.Ba(OH)2·8H2O和NH4Cl固体反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com