


科目:高中化学 来源: 题型:
 过氧化银(Ag2O2)是银锌碱性电池正极的活性物质,可通过下列反应制备:
过氧化银(Ag2O2)是银锌碱性电池正极的活性物质,可通过下列反应制备:查看答案和解析>>
科目:高中化学 来源: 题型:
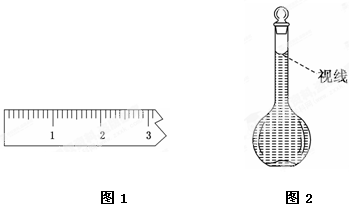
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
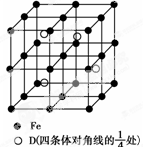 A、B、C、D分别代表四种不同的短周期元素.A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的p亚层中有1个电子.
A、B、C、D分别代表四种不同的短周期元素.A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的p亚层中有1个电子.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Cu2+、NO3-、SO32- |
| B、K+、Na+、Cl-、SiO32- |
| C、Al3+、NH4+、NO3-、Cl- |
| D、K+、Na+、AlO2-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖的结构简式:CH2OH(CHOH)4CHO |
B、聚丙烯的结构简式: |
C、Cl-的结构示意图: |
D、甲烷的球棍模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuCl2[CuSO4] |
| B、NaCl[HCl] |
| C、NaOH[NaOH] |
| D、CuSO4[Cu(OH)2] |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com