
分析 (1)纤维素为多糖,水解最终产物为葡萄糖(C6H12O6),具有还原性,可将NaClO3还原得到ClO2.Cl从+5到+4价,降低1价,葡萄糖(C6H12O6)C均价为0,到+4价,升高4价,然后配平得到;由配平的化学方程式可知生成24molClO2和6mol CO2气体转移24mol的电子;
(2)依据m=nM计算需要的氢氧化钠溶质的质量,配制溶液需要天平称量固体质量,精确到0.1g,若实验时需要450mL 4mol/L的NaOH溶液,需要取用500ml容量瓶中配制,所使用的仪器除托盘天平、胶头滴管、玻璃棒外,还含有烧杯和500ml容量瓶,
A.称量固体时动作缓慢,可能导致氢氧化钠吸收水蒸气和空气中的二氧化碳,导致溶质减小;
B.容量瓶未干燥立即用来配制溶液对配制溶液的结果无影响;
C.NaOH固体溶解后溶液温度升高,立刻转移溶液温度升高,常温下溶液浓度增大;
D.在容量瓶中定容时俯视容量瓶刻度线,液面倍提高,定容未达到刻度;
E.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线,溶液浓度减小;
解答 解:(1)纤维素为多糖,水解最终产物为葡萄糖(C6H12O6),具有还原性,可将NaClO3还原得到ClO2.Cl从+5到+4价,降低1价,葡萄糖(C6H12O6)C均价为0,到+4价,升高4价,则配平后的化学方程式为1 C6H12O6+24NaClO3+12H2SO4=24ClO2↑+6CO2↑+18H2O+12Na2SO4,电子转移的方向和数目表示为: ,
,
30mol的气体~24mole-
30×22.4L 24mol
1.12L 0.16mol 所以转移电子数为0.04NA,
故答案为:1;C6H12O6;24;6;12;Na2SO4; ;0.04NA;
;0.04NA;
(2)实验时需要450mL 4mol/L的NaOH溶液,需要取用500ml容量瓶中配制,配制溶液需要天平称量固体质量,精确到0.1g,依据m=nM计算需要的氢氧化钠溶质的质量=0.5L×4mol/L×40g/mol=80.0g,若实验时需要450mL 4mol/L的NaOH溶液,需要取用500ml容量瓶中配制,所使用的仪器除托盘天平、胶头滴管、玻璃棒外,还含有烧杯和500ml容量瓶;
A.称量固体时动作缓慢,可能导致氢氧化钠吸收水蒸气和空气中的二氧化碳,导致溶质减小,测定结果偏低,故A错误;
B.最后配制溶液需要加入水定容,容量瓶未干燥立即用来配制溶液对配制溶液的结果无影响,故B错误;
C.NaOH固体溶解后溶液温度升高,立刻转移溶液温度升高,常温下液面未达到刻度,溶液浓度增大,故C正确;
D.在容量瓶中定容时俯视容量瓶刻度线,液面倍提高,定容未达到刻度,溶液浓度增大,故D正确;
E.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线,水加入超出刻度线,溶液浓度减小,故E错误;
故答案为:CD.
故答案为:80.0;500mL容量瓶、烧杯;CD.
点评 本题考查了氧化还原反应电子转移,电子守恒计算分析,化学方程式书写,溶液配制方法和过程分析应用,掌握基础是解题关键,题目难度中等.


 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源: 题型:选择题
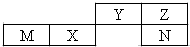 五种短周期元素在元素周期表中的位置如图,其中只有一种为金属元素.下列说法正确的是( )
五种短周期元素在元素周期表中的位置如图,其中只有一种为金属元素.下列说法正确的是( )| A. | 简单离子半径大小:M>N>Z | |
| B. | 最简单气态氢化物的沸点高低:N>Z>Y | |
| C. | M的最高价氧化物可与N的最高价氧化物对应水化物反应 | |
| D. | N单质可与Z的最简单氢化物反应置换出Z单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
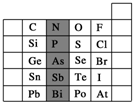 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | PH值一定为5 | B. | 一定是酸溶液 | ||
| C. | 可能是强酸的酸式盐溶液 | D. | PH值可能为9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸中逐滴加入食盐溶液 | B. | 硫酸中逐滴加入氢氧化钠溶液 | ||
| C. | 石灰乳中滴加稀盐酸 | D. | 硫酸中逐滴加入氢氧化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+的电子排布图: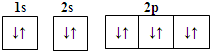 | B. | Na+的结构示意图: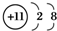 | ||
| C. | Cr的价层电子排布式:3d54s1 | D. | C的电子排布式:1s22s12p3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
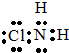 ,从物质结构的角度解释两者熔点相差较大的原因氯胺NH2Cl为分子晶体,NH4Cl为离子晶体,熔沸点离子晶体高于分子晶体.
,从物质结构的角度解释两者熔点相差较大的原因氯胺NH2Cl为分子晶体,NH4Cl为离子晶体,熔沸点离子晶体高于分子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水是强电解质 | B. | 25℃时,纯水的pH=7 | ||
| C. | 可燃冰是可以燃烧的水 | D. | 氢氧两种元素只能组成水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com