
| A、氯化氢不易分解 |
| B、液态氯化氢不导电 |
| C、氯化氢溶于水发生电离 |
| D、氯化氢水溶液显酸性 |


科目:高中化学 来源: 题型:
| A、通常状况下,干燥的氯气能和Fe反应 |
| B、红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
| C、纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状 |
| D、氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
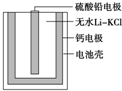 如图为一种热激活电池的基本结构,该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.作为电解质的无水LiClKCl混合物受热熔融后,电池即可瞬间输出电能.下列有关说法正确的是( )
如图为一种热激活电池的基本结构,该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.作为电解质的无水LiClKCl混合物受热熔融后,电池即可瞬间输出电能.下列有关说法正确的是( )| A、正极反应式:Ca+2Cl-+2e-═CaCl2 |
| B、放电过程中,Li+向负极移动 |
| C、每转移0.1mol电子,理论上生成20.7gPb |
| D、常温时,在正负极间接上电流表或检流计,指针不偏转 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气溶于水形成的溶液能导电,故氯气是电解质 |
| B、没有氧元素参加的反应一定不是氧化还原反应 |
| C、在水中能电离出H+的化合物一定是酸 |
| D、有单质生成的分解反应一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.4g | B、3.2g |
| C、6.4g | D、9.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠投入到水中:2Na+2H2O=2Na++OH-+H2↑ | ||||
B、实验室制氯气:MnO2+2H++2Cl-
| ||||
| C、铜与浓硫酸反应:Cu+2H+=Cu2++H2↑ | ||||
| D、金属铝投入氢氧化钠溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:
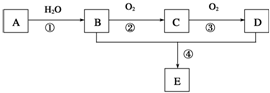 已知A是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如图所示.
已知A是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com